Biochimica del dolore:Tutte le sindromi dolorose hanno un profilo infiammatorio. Un profilo infiammatorio può variare da persona a persona e può anche variare in una persona in momenti diversi. Il trattamento delle sindromi dolorose consiste nel comprendere questo profilo infiammatorio. Le sindromi dolorose sono trattate da un punto di vista medico, chirurgico o entrambi. L'obiettivo è inibire / sopprimere la produzione di mediatori infiammatori. E un risultato positivo è quello che si traduce in meno infiammazione e ovviamente meno dolore.
Contenuti
Biochimica del dolore
Obiettivi:
- Chi sono i giocatori chiave
- Quali sono i meccanismi biochimici?
- Quali sono le conseguenze?
Recensione di infiammazione:
Giocatori chiave
 Perché mi fa male la spalla? Una rassegna delle basi neuroanatomiche e biochimiche del dolore alla spalla
Perché mi fa male la spalla? Una rassegna delle basi neuroanatomiche e biochimiche del dolore alla spalla
ABSTRACT
Se un paziente chiede `` perché mi fa male la spalla? '', La conversazione si sposterà rapidamente sulla teoria scientifica e talvolta su congetture prive di fondamento. Spesso, il clinico diventa consapevole dei limiti delle basi scientifiche della loro spiegazione, dimostrando l'incompletezza della nostra comprensione della natura del dolore alla spalla. Questa revisione adotta un approccio sistematico per aiutare a rispondere a domande fondamentali relative al dolore alla spalla, al fine di fornire approfondimenti sulla ricerca futura e nuovi metodi per il trattamento del dolore alla spalla. Esploreremo i ruoli di (1) i recettori periferici, (2) l'elaborazione del dolore periferico o nocicezione , (3) il midollo spinale, (4) il cervello, (5) la posizione dei recettori nella spalla e (6 ) l'anatomia neurale della spalla. Consideriamo anche come questi fattori possano contribuire alla variabilità nella presentazione clinica, nella diagnosi e nel trattamento del dolore alla spalla. In questo modo miriamo a fornire una panoramica delle parti componenti del sistema di rilevamento del dolore periferico e dei meccanismi centrali di elaborazione del dolore nel dolore alla spalla che interagiscono per produrre dolore clinico.
INTRODUZIONE: UNA STORIA MOLTO BREVE DI SCIENZA DEL DOLORE ESSENZIALE PER I CLINICI
La natura del dolore, in generale, è stata oggetto di molte controversie nel secolo scorso. Nel 17 ° secolo la teoria di Descartes1 propose che l'intensità del dolore fosse direttamente correlata alla quantità di lesione tissutale associata e che il dolore fosse elaborato in un percorso distinto. Molte teorie precedenti si basavano su questa cosiddetta filosofia cartesiana "dualista", vedendo il dolore come la conseguenza della stimolazione di un recettore del dolore periferico "specifico" nel cervello. Nel 20 ° secolo seguì una battaglia scientifica tra due teorie opposte, vale a dire la teoria della specificità e la teoria dei modelli. La `` teoria della specificità '' cartesiana vedeva il dolore come una modalità specifica separata di input sensoriale con il proprio apparato, mentre la `` teoria dei modelli '' riteneva che il dolore fosse il risultato dell'intensa stimolazione di recettori non specifici.2 Nel 1965, Wall e Melzack 3 La teoria del cancello del dolore ha fornito prove per un modello in cui la percezione del dolore era modulata sia dal feedback sensoriale che dal sistema nervoso centrale. Un altro enorme progresso nella teoria del dolore più o meno nello stesso periodo ha visto la scoperta della modalità di azione specifica degli oppioidi.4 Successivamente, i recenti progressi nella neuroimaging e nella medicina molecolare hanno notevolmente ampliato la nostra comprensione generale del dolore.
Quindi come si collega al dolore alla spalla? Il dolore alla spalla è un problema clinico comunee una solida comprensione del modo in cui il dolore viene elaborato dal corpo è essenziale per diagnosticare e trattare al meglio il dolore di un paziente. I progressi nella nostra conoscenza dell'elaborazione del dolore promettono di spiegare la mancata corrispondenza tra patologia e percezione del dolore, possono anche aiutarci a spiegare perché alcuni pazienti non rispondono a determinati trattamenti.
BLOCCHI DI COSTRUZIONE BASE DI DOLORE
Recettori sensoriali periferici: il meccanorecettore e l '' innocicettore '
Esistono numerosi tipi di recettori sensoriali periferici presenti nel sistema muscolo-scheletrico umano. 5 Possono essere classificati in base alla loro funzione (come meccanocettori, termocettori o nocicettori) o morfologia (terminazioni nervose libere o diversi tipi di recettori incapsulati) 5 I diversi tipi di recettori possono quindi essere ulteriormente sottoclassificati in base a la presenza di alcuni marcatori chimici. Ci sono sovrapposizioni significative tra diverse classi funzionali di recettori, per esempio
Elaborazione del dolore periferico: "Notociception"
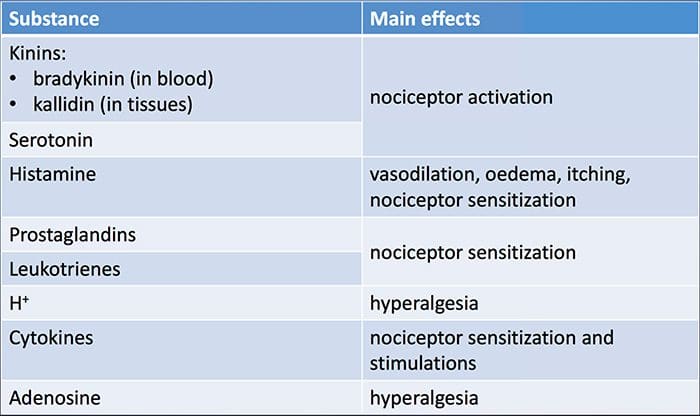
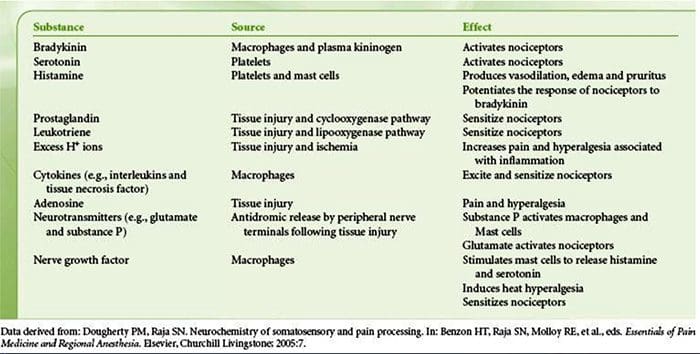
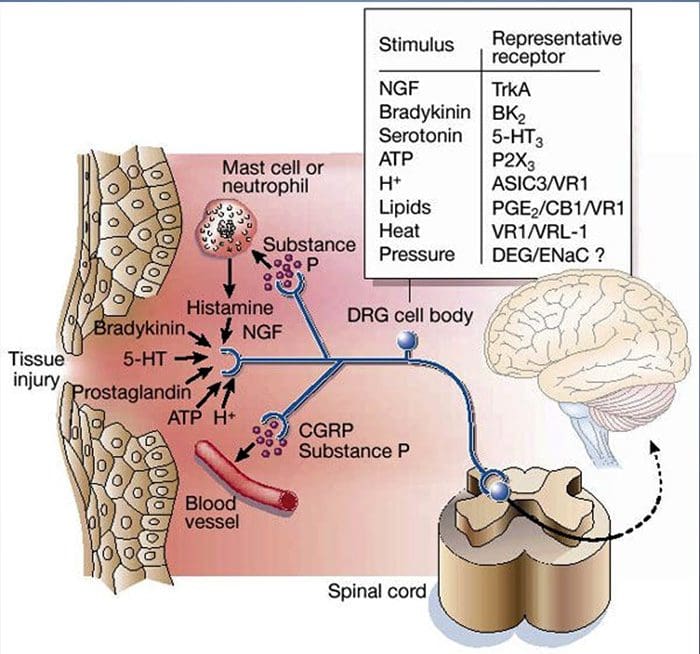
Il danno tissutale coinvolge una varietà di mediatori infiammatori che vengono rilasciati da cellule danneggiate tra cui bradichinina, istamina, 5-idrossitriptamina, ATP, ossido nitrico e alcuni ioni (K + e H +). L'attivazione della via dell'acido arachidonico porta alla produzione di prostaglandine, trombossani e leucotrieni. Anche le citochine, comprese le interleuchine e il fattore di necrosi tumorale ?, e le neurotrofine, come il fattore di crescita nervoso (NGF), vengono rilasciate e sono intimamente coinvolte nella facilitazione dell'infiammazione.15 Altre sostanze come gli amminoacidi eccitatori (glutammato) e gli oppioidi ( endotelina-1) sono stati anche implicati nella risposta infiammatoria acuta.16 17 Alcuni di questi agenti possono attivare direttamente nocicettori, mentre altri determinano il reclutamento di altre cellule che poi rilasciano ulteriori agenti facilitatori.18 Questo processo locale che determina una maggiore reattività di neuroni nocicettivi al loro normale input e / o il reclutamento di una risposta a input normalmente sottosoglia è definito `` sensibilizzazione periferica ''. La Figura 1 riassume alcuni dei meccanismi chiave coinvolti.
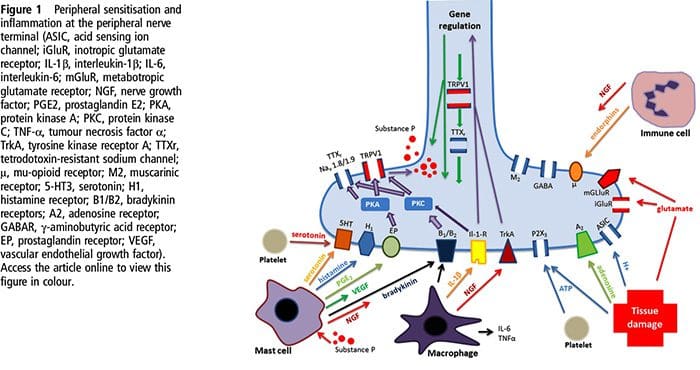 NGF e il recettore transitorio del potenziale recettore del canale cationico sottofamiglia V membro 1 (TRPV1) hanno una relazione simbiotica quando si tratta di infiammazione e sensibilizzazione dei nocicettori. Le citochine prodotte nel tessuto infiammato determinano un aumento della produzione di NGF.19 L'NGF stimola il rilascio di istamina e serotonina (5-HT3) da parte dei mastociti e sensibilizza anche i nocicettori, alterando eventualmente le proprietà di A? fibre tali che una percentuale maggiore diventa nocicettiva. Il recettore TRPV1 è presente in una sottopopolazione di fibre afferenti primarie ed è attivato da capsaicina, calore e protoni. Il recettore TRPV1 è sintetizzato nel corpo cellulare della fibra afferente e viene trasportato sia al terminale periferico che a quello centrale, dove contribuisce alla sensibilità delle afferenze nocicettive. L'infiammazione provoca la produzione periferica di NGF che si lega quindi al recettore della tirosin chinasi di tipo 1 sui terminali dei nocicettori, l'NGF viene quindi trasportato al corpo cellulare dove porta a una regolazione della trascrizione di TRPV1 e di conseguenza aumenta la sensibilità dei nocicettori.19 20 NGF e altri mediatori infiammatori sensibilizzano anche TRPV1 attraverso una vasta gamma di vie di messaggistica secondarie. Si ritiene che molti altri recettori, inclusi i recettori colinergici, i recettori dell'acido α-aminobutirrico (GABA) e i recettori della somatostatina, siano coinvolti nella sensibilità dei nocicettori periferici.
NGF e il recettore transitorio del potenziale recettore del canale cationico sottofamiglia V membro 1 (TRPV1) hanno una relazione simbiotica quando si tratta di infiammazione e sensibilizzazione dei nocicettori. Le citochine prodotte nel tessuto infiammato determinano un aumento della produzione di NGF.19 L'NGF stimola il rilascio di istamina e serotonina (5-HT3) da parte dei mastociti e sensibilizza anche i nocicettori, alterando eventualmente le proprietà di A? fibre tali che una percentuale maggiore diventa nocicettiva. Il recettore TRPV1 è presente in una sottopopolazione di fibre afferenti primarie ed è attivato da capsaicina, calore e protoni. Il recettore TRPV1 è sintetizzato nel corpo cellulare della fibra afferente e viene trasportato sia al terminale periferico che a quello centrale, dove contribuisce alla sensibilità delle afferenze nocicettive. L'infiammazione provoca la produzione periferica di NGF che si lega quindi al recettore della tirosin chinasi di tipo 1 sui terminali dei nocicettori, l'NGF viene quindi trasportato al corpo cellulare dove porta a una regolazione della trascrizione di TRPV1 e di conseguenza aumenta la sensibilità dei nocicettori.19 20 NGF e altri mediatori infiammatori sensibilizzano anche TRPV1 attraverso una vasta gamma di vie di messaggistica secondarie. Si ritiene che molti altri recettori, inclusi i recettori colinergici, i recettori dell'acido α-aminobutirrico (GABA) e i recettori della somatostatina, siano coinvolti nella sensibilità dei nocicettori periferici.
Un gran numero di mediatori dell'infiammazione sono stati specificamente implicati nel dolore alla spalla e nella malattia della cuffia dei rotatori.21 Mentre alcuni mediatori chimici attivano direttamente i nocicettori, la maggior parte porta a cambiamenti nel neurone sensoriale stesso piuttosto che attivarlo direttamente. Questi cambiamenti possono dipendere dalla trascrizione post-traduzionale precoce o ritardata. Esempi del primo sono i cambiamenti nel recettore TRPV25 o nei canali ionici voltaggio-dipendenti risultanti dalla fosforilazione delle proteine legate alla membrana. Esempi di questi ultimi includono l'aumento indotto da NGF nella produzione del canale TRV1 e l'attivazione indotta dal calcio di fattori di trascrizione intracellulare.
Meccanismi molecolari di nocicezione
La sensazione di dolore ci avverte di lesioni reali o imminenti e innesca risposte protettive appropriate. Sfortunatamente, il dolore spesso sopravvive alla sua utilità come sistema di allarme e invece diventa cronico e debilitante. Questa transizione a una fase cronica comporta cambiamenti all'interno del midollo spinale e del cervello, ma c'è anche una notevole modulazione in cui i messaggi di dolore vengono avviati - a livello del neurone sensoriale primario. Gli sforzi per determinare come questi neuroni rilevano stimoli che producono dolore di natura termica, meccanica o chimica hanno rivelato nuovi meccanismi di segnalazione e ci hanno avvicinato alla comprensione degli eventi molecolari che facilitano le transizioni dal dolore acuto a quello persistente.
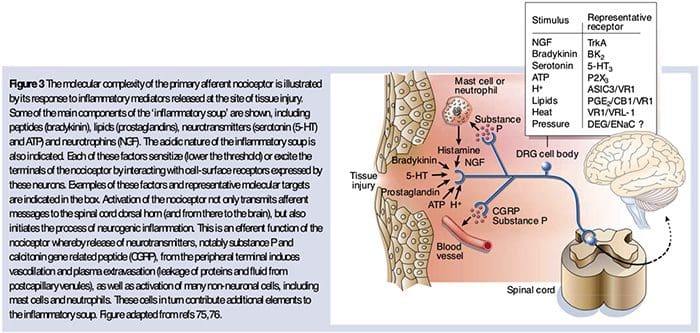 La neurochimica dei nocicettori
La neurochimica dei nocicettori
Il glutammato è il neurotrasmettitore eccitatorio predominante in tutti i nocicettori. Gli studi istochimici del DRG adulto, tuttavia, rivelano due ampie classi di fibra C non mielinizzata.
Trasduttori chimici per peggiorare il dolore
Come descritto sopra, il danno accresce la nostra esperienza dolorosa aumentando la sensibilità dei nocicettori agli stimoli sia termici che meccanici. Questo fenomeno deriva, in parte, dalla produzione e dal rilascio di mediatori chimici dal terminale sensoriale primario e da cellule non neurali (ad esempio, fibroblasti, mastociti, neutrofili e piastrine) nell'ambiente36 (Figura 3). Alcuni componenti del brodo infiammatorio (ad esempio protoni, ATP, serotonina o lipidi) possono alterare l'eccitabilità neuronale direttamente interagendo con i canali ionici sulla superficie del nocicettore, mentre altri (ad esempio, bradichinina e NGF) si legano ai recettori metabotropici e mediare i loro effetti attraverso le cascate di segnalazione secondo messenger11. Sono stati fatti notevoli progressi nella comprensione delle basi biochimiche di tali meccanismi modulatori.
Protoni extracellulari e acidosi dei tessuti
L'acidosi tessutale locale è una tipica risposta fisiologica alle lesioni e il grado di dolore o disagio associato è ben correlato con la grandezza dell'acidificazione37. L'applicazione di acido (pH 5) alla pelle produce scarichi sostenuti in un terzo o più dei nocicettori polimodali che innervano il campo recettivo 20.
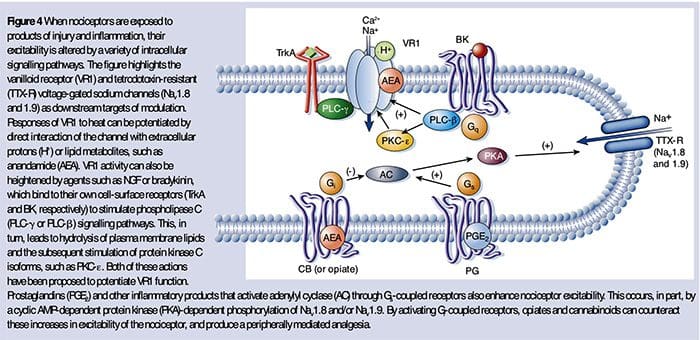 Meccanismi cellulari e molecolari del dolore
Meccanismi cellulari e molecolari del dolore
Astratto
Il sistema nervoso rileva e interpreta una vasta gamma di stimoli termici e meccanici nonché sostanze irritanti chimiche ambientali ed endogene. Quando sono intensi, questi stimoli generano dolore acuto e, nel contesto di una lesione persistente, le componenti del sistema nervoso sia periferico che centrale del sistema di trasmissione del dolore mostrano una plasticità tremenda, aumentando i segnali del dolore e producendo ipersensibilità. Quando la plasticità facilita i riflessi protettivi, può essere utile, ma quando i cambiamenti persistono, può verificarsi una condizione di dolore cronico. Studi genetici, elettrofisiologici e farmacologici stanno chiarendo i meccanismi molecolari che sono alla base della rilevazione, della codifica e della modulazione di stimoli nocivi che generano dolore.
Introduzione: dolore acuto e persistente
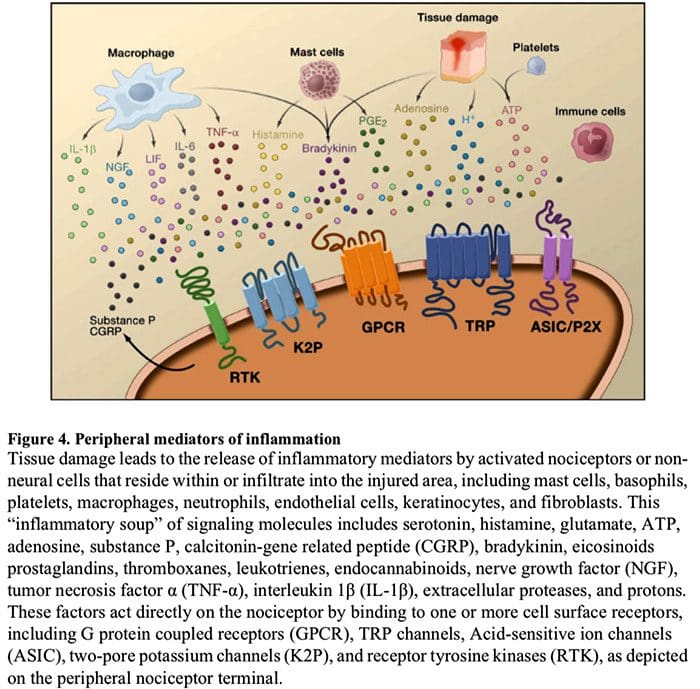
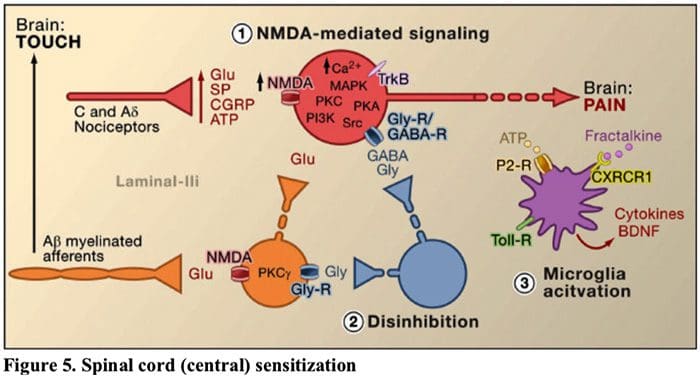 Figura 5. Sensibilizzazione al midollo spinale (centrale)
Figura 5. Sensibilizzazione al midollo spinale (centrale)
- Sensibilizzazione al recettore mediata da glutammato / NMDA.A seguito di stimolazione intensa o lesioni persistenti, C e A attivati? i nocicettori rilasciano una varietà di neurotrasmettitori tra cui dlutammato, sostanza P, peptide correlato al gene della calcitonina (CGRP) e ATP, sui neuroni di uscita nella lamina I del corno dorsale superficiale (rosso). Di conseguenza, i recettori del glutammato NMDA normalmente silenti situati nel neurone postsinaptico possono ora segnalare, aumentare il calcio intracellulare e attivare una serie di vie di segnalazione dipendenti dal calcio e secondi messaggeri tra cui la proteina chinasi attivata dal mitogeno (MAPK), la protein chinasi C (PKC) , proteina chinasi A (PKA) e Src. Questa cascata di eventi aumenterà l'eccitabilità del neurone di output e faciliterà la trasmissione dei messaggi di dolore al cervello.
- Disinibizione.In circostanze normali, gli interneuroni inibitori (blu) rilasciano continuamente GABA e / o glicina (Gly) per diminuire l'eccitabilità dei neuroni di uscita della lamina I e modulare la trasmissione del dolore (tono inibitorio). Tuttavia, nel contesto della lesione, questa inibizione può essere persa, con conseguente iperalgesia. Inoltre, la disinibizione può abilitare mielinizzati A non nocicettivi? afferenze primarie per attivare i circuiti di trasmissione del dolore in modo tale che gli stimoli normalmente innocui vengono ora percepiti come dolorosi. Ciò avviene, in parte, attraverso la disinibizione della PKC eccitatoria? esprimendo interneuroni nella lamina interna II.
- Attivazione microglialeLa lesione del nervo periferico promuove il rilascio di ATP e della chemochina fractalkine che stimolerà le cellule microgliali. In particolare, l'attivazione dei recettori purinergici, CX3CR1 e Toll-like sulla microglia (viola) si traduce nel rilascio del fattore neurotrofico derivato dal cervello (BDNF), che attraverso l'attivazione dei recettori TrkB espressi dai neuroni di uscita della lamina I, promuove una maggiore eccitabilità e aumento del dolore in risposta alla stimolazione sia nociva che innocua (cioè iperalgesia e allodinia). La microglia attivata rilascia anche una serie di citochine, come il fattore di necrosi tumorale? (TNF?), Interleuchina-1? e 6 (IL-1 ?, IL-6) e altri fattori che contribuiscono alla sensibilizzazione centrale.
Il milieu chimico di infiammazione
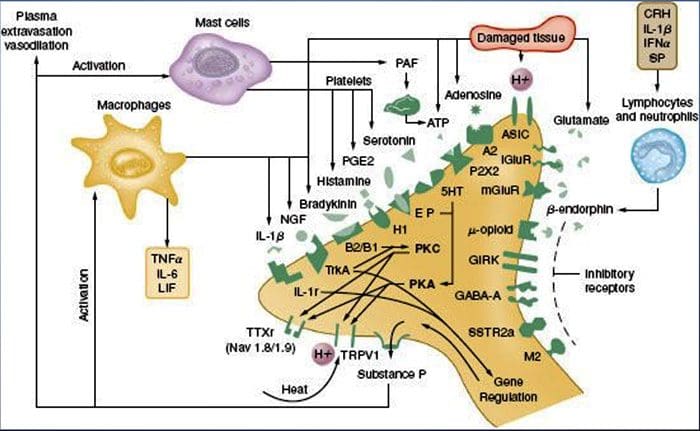
La sensibilizzazione periferica più comunemente deriva da cambiamenti associati all'infiammazione nell'ambiente chimico della fibra nervosa (McMahon et al., 2008). Pertanto, il danno tissutale è spesso accompagnato dall'accumulo di fattori endogeni rilasciati da nocicettori attivati o cellule non neurali che risiedono all'interno o si infiltrano nell'area danneggiata (inclusi mastociti, basofili, piastrine, macrofagi, neutrofili, cellule endoteliali, cheratinociti e fibroblasti). Collettivamente. questi fattori, denominati `` zuppa infiammatoria '', rappresentano una vasta gamma di molecole di segnalazione, inclusi neurotrasmettitori, peptidi (sostanza P, CGRP, bradichinina), eicosinoidi e lipidi correlati (prostaglandine, trombossani, leucotrieni, endocannabinoidi), neurotrofine, citochine e chemochine, così come proteasi e protoni extracellulari. Sorprendentemente, i nocicettori esprimono uno o più recettori della superficie cellulare in grado di riconoscere e rispondere a ciascuno di questi agenti pro-infiammatori o pro-algesici (Figura 4). Tali interazioni aumentano l'eccitabilità della fibra nervosa, aumentando così la sua sensibilità alla temperatura o al tatto.
Indiscutibilmente l'approccio più comune per ridurre il dolore infiammatorio comporta l'inibizione della sintesi o dell'accumulo di componenti del brodo infiammatorio. Questo è meglio esemplificato da farmaci antinfiammatori non steroidei, come l'aspirina o l'ibuprofene, che riducono il dolore infiammatorio e l'iperalgesia inibendo le cicloossigenasi (Cox-1 e Cox-2) coinvolte nella sintesi delle prostaglandine. Un secondo approccio consiste nel bloccare le azioni degli agenti infiammatori al nocicettore. Qui, evidenziamo esempi che forniscono nuove informazioni sui meccanismi cellulari di sensibilizzazione periferica o che costituiscono la base di nuove strategie terapeutiche per il trattamento del dolore infiammatorio.
L'NGF è forse meglio conosciuto per il suo ruolo come fattore neurotrofico necessario per la sopravvivenza e lo sviluppo dei neuroni sensoriali durante l'embriogenesi, ma nell'adulto, NGF è anche prodotto nel contesto di danno tissutale e costituisce una componente importante del brodo infiammatorio (Ritner et al., 2009). Tra i suoi numerosi bersagli cellulari, NGF agisce direttamente sui nocicettori della fibra C peptidergici, che esprimono la tirosin-chinasi del recettore NGF ad alta affinità, TrkA, così come il recettore della neurotropina a bassa affinità, p75 (Chao, 2003; Snider and McMahon, 1998). NGF produce una profonda ipersensibilità al calore e agli stimoli meccanici attraverso due meccanismi distinti temporalmente. Inizialmente, un'interazione NGF-TrkA attiva le vie di segnalazione a valle, tra cui la fosfolipasi C (PLC), la chinasi proteica attivata dal mitogeno (MAPK) e il fosfoinositide 3-chinasi (PI3K). Ciò si traduce in un potenziamento funzionale delle proteine bersaglio nel terminale periferico dei nocicettori, in particolare TRPV1, che porta a un rapido cambiamento della sensibilità al calore cellulare e comportamentale (Chuang et al., 2001).
Indipendentemente dai loro meccanismi pro-nocicettivi, l'interferenza con la segnalazione di neurotrofine o citochine è diventata una strategia importante per il controllo della malattia infiammatoria o del dolore risultante. L'approccio principale prevede il blocco di NGF o TNF-? azione con un anticorpo neutralizzante. Nel caso del TNF-?, Questo è stato notevolmente efficace nel trattamento di numerose malattie autoimmuni, inclusa l'artrite reumatoide, portando a una drastica riduzione sia della distruzione dei tessuti che dell'iperalgesia di accompagnamento (Atzeni et al., 2005). Poiché le principali azioni di NGF sul nocicettore adulto si verificano nel contesto dell'infiammazione, il vantaggio di questo approccio è che l'iperalgesia diminuirà senza influire normale percezione del dolore. Infatti, gli anticorpi anti-NGF sono attualmente in studi clinici per il trattamento delle sindromi da dolore infiammatorio (Hefti et al., 2006).
Sensibilizzazione mediata dal recettore glutammato / NMDA
Il dolore acuto è segnalato dal rilascio di glutammato dai terminali centrali dei nocicettori, generando correnti eccitatorie post-sinaptiche (EPSC) in neuroni del corno dorsale di secondo ordine. Ciò si verifica principalmente attraverso l'attivazione di AMPA postsinaptici e sottotipi di kainato di recettori del glutammato ionotropico. La sommatoria degli EPSC sub-soglia nel neurone postsinaptico finirà per provocare un potenziale di azione e la trasmissione del messaggio del dolore ai neuroni di ordine superiore.
Altri studi indicano che i cambiamenti nel neurone di proiezione, di per sé, contribuiscono al processo di inibizione. Ad esempio, la lesione del nervo periferico regola in modo profondo il trasportatore K + - Cl- KCC2, che è essenziale per mantenere i gradienti normali di K + e Cl attraverso la membrana plasmatica (Coull et al., 2003). La downregolazione del KCC2, che è espressa nei neuroni di proiezione della lamina I, determina uno spostamento del gradiente Cl, tale che l'attivazione dei recettori GABA-A depolarizza, piuttosto che iperpolarizzare i neuroni di proiezione della lamina I. Ciò, a sua volta, aumenterebbe l'eccitabilità e aumenterebbe la trasmissione del dolore. Infatti, il blocco farmacologico o la downregulation mediata da siRNA di KCC2 nel ratto induce allodinia meccanica.
Fonte:
Perché mi fa male la spalla? Una revisione delle basi neuroanatomiche e biochimiche del dolore alla spalla
Benjamin John Floyd Dean, Stephen Edward Gwilym, Andrew Jonathan Carr
Meccanismi cellulari e molecolari del dolore
Allan I. Basbaum1, Diana M. Bautista2, Gre? Gory Scherrer1 e David Julius3
1Department of Anatomy, Università della California, San Francisco 94158
2Dipartimento di Biologia Molecolare e Cellulare, Università della California, Berkeley CA 94720 3Dipartimento di Fisiologia, Università della California, San Francisco 94158
Meccanismi molecolari della nocicezione
David Julius * e Allan I. Basbaum
*Dipartimento di Farmacologia Cellulare e Molecolare e �Dipartimenti di Anatomia e Fisiologia e WM Keck Foundation Center for Integrative Neuroscience, University of California San Francisco, San Francisco, California 94143, USA (e-mail: julius@socrates.ucsf.edu)
Le informazioni qui riportate su "Biochimica del dolore" non intende sostituire un rapporto individuale con un professionista sanitario qualificato o un medico autorizzato e non è una consulenza medica. Ti incoraggiamo a prendere decisioni sanitarie basate sulla tua ricerca e collaborazione con un professionista sanitario qualificato.
Informazioni sul blog e discussioni sull'ambito
Il nostro ambito informativo è limitato a chiropratica, muscolo-scheletrico, medicine fisiche, benessere, contributo eziologico disturbi viscerosomatici all'interno di presentazioni cliniche, dinamiche cliniche associate ai riflessi somatoviscerali, complessi di sublussazione, problemi di salute sensibili e/o articoli, argomenti e discussioni di medicina funzionale.
Forniamo e presentiamo collaborazione clinica con specialisti di varie discipline. Ogni specialista è regolato dal proprio ambito di pratica professionale e dalla propria giurisdizione di licenza. Utilizziamo protocolli funzionali di salute e benessere per trattare e supportare la cura delle lesioni o dei disturbi del sistema muscolo-scheletrico.
I nostri video, post, argomenti, soggetti e approfondimenti trattano questioni cliniche, problemi e argomenti che riguardano e supportano direttamente o indirettamente il nostro ambito di pratica clinica.*
Il nostro ufficio ha ragionevolmente tentato di fornire citazioni di supporto e ha identificato lo studio o gli studi di ricerca pertinenti a sostegno dei nostri post. Forniamo copie degli studi di ricerca di supporto a disposizione degli organi di regolamentazione e del pubblico su richiesta.
Comprendiamo che copriamo questioni che richiedono una spiegazione aggiuntiva su come può essere d'aiuto in un particolare piano di assistenza o protocollo di trattamento; pertanto, per discutere ulteriormente l'argomento di cui sopra, non esitate a chiedere Dott. Alex Jimenez, DC, o contattaci al 915-850-0900.
Siamo qui per aiutare te e la tua famiglia.
Blessings
Il dottor Alex Jimenez DC MSACP, Marina Militare*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionalmedicine.com
Licenza come Dottore in Chiropratica (DC) in Texas & Nuovo Messico*
Licenza Texas DC n. TX5807, Licenza DC del New Mexico n. NM-DC2182
Autorizzato come infermiere registrato (RN*) in Florida
Licenza Florida Licenza RN # RN9617241 (controllo n. 3558029)
Stato compatto: Licenza multistato: Autorizzato ad esercitare in Stati 40*
Dott. Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Il mio biglietto da visita digitale







