1. CHI. CHI | Sovrappeso e obesità. www.who.int/gho/ncd/
risk_factors / sovrappeso / it / index.html. Accesso a 29 gennaio 2015.
2. Visscher PM, Brown MA, McCarthy MI, Yang J. Cinque anni di scoperta di GWAS.
Sono J Hum Genet. 2012; 90: 7.
3. Locke AE, Kahali B, Berndt SI, giustizia AE, Pers TH, giorno FR, et al. Genetico
gli studi sull'indice di massa corporea forniscono nuove conoscenze per la biologia dell'obesità. Natura.
2015; 518: 197 206.
4. Ling C, Del Guerra S, Lupi R, Rnn T, Granhall C, Luthman H, et al.
Regolazione epigenetica di PPARGC1A in isole diabetiche di tipo 2 umano e
effetto sulla secrezione di insulina. Diabetologia. 2008; 51: 615-22.
5. Van Dijk SJ, Molloy PL, Varinli H, Morrison JL, Muhlhausler BS. L'epigenetica
e l'obesità umana. Int J Obes (Lond). 2015; 39: 85 97.
6. Teh AL, Pan H, Chen L, Ong ML, Dogra S, Wong J, et al. L'effetto di
genotipo e nell'utero ambiente sulla variabilità interindividuale nel neonato
Metilomi del DNA. Genome Res. 2014; 24: 1064 74.
7. Olsson AH, Volkov P, Bacos K, Dayeh T, Hall E, Nilsson EA, et al. genomewide
associazioni tra influenza genetica e variazioni epigenetiche
l'espressione di mRNA e la secrezione di insulina negli isolotti pancreatici umani. PLoS
Genet. 2014; 10: e1004735.
8. Grundberg E, Meduri E, Sandling JK, Hedman AK, Keildson S, Buil A, et al.
Analisi globale della variazione della metilazione del DNA nel tessuto adiposo dai gemelli
rivela i collegamenti alle varianti associate alle malattie negli elementi regolatori distali.
Sono J Hum Genet. 2013; 93: 876.
9. Ronn T, Volkov P, Gillberg L, Kokosar M, Perfilyev A, Jacobsen AL, et al.
Impatto dell'età, dei livelli BMI e HbA1c sul DNA genoma-wide
metilazione e espressione di espressione di mRNA nel tessuto adiposo umano
e l'identificazione di biomarcatori epigenetici nel sangue. Hum Mol Genet.
2015; 24: 3792 813.
10. Waterland RA, Michels KB. Epidemiologia epigenetica dello sviluppo
ipotesi delle origini. Annu Rev Nutr. 2007; 27: 363.
11. McMillen IC, Rattanatray L, Duffield JA, Morrison JL, MacLaughlin SM, Gentili
S, et al. Le prime origini dell'obesità successiva: percorsi e meccanismi. adv
Exp Med Biol. 2009; 646: 71.
12. Ravelli A, van der Meulen J, Michels R, Osmond C, Barker D, Hales C, et al.
Tolleranza al glucosio negli adulti dopo l'esposizione prenatale alla carestia. Lancetta.
1998; 351: 173 7.
13. McMillen IC, MacLaughlin SM, Muhlhausler BS, Gentili S, Duffield JL,
Morrison JL. Origini dello sviluppo della salute e della malattia degli adulti: il ruolo di
la nutrizione periconceptional e fetale. Basic Clin Pharmacol Toxicol.
2008; 102: 82 9.
14. Zhang S, Rattanatray L, McMillen IC, Suter CM, Morrison JL. periconcezionale
la nutrizione e la programmazione precoce di una vita di obesità o avversità. Prog
Biophys Mol Biol. 2011; 106: 307-14.
15. Bouret S, Levin BE, Ozanne SE. Controllo delle interazioni genico-ambiente
l'energia e l'omeostasi del glucosio e le origini dello sviluppo dell'obesità.
Physiol Rev.2015; 95: 47 82.
16. Borengasser SJ, Zhong Y, Kang P, Lindsey F, Ronis MJ, Badger TM, et al.
L'obesità materna aumenta la differenziazione e l'alterazione del tessuto adiposo bianco
metilazione di DNA su scala genoma in prole di topo maschile. Endocrinologia.
2013; 154: 4113 25.
17. Gluckman PD, Lillycrop KA, Vickers MH, Pleasants AB, Phillips ES, Beedle AS,
et al. La plasticità metabolica durante lo sviluppo dei mammiferi è orientata
dipendente dal primo stato nutrizionale. Proc Natl Acad Sci US A.
2007; 104: 12796 800.
18. Godfrey KM, Sheppard A, Gluckman PD, Lillycrop KA, Burdge GC, McLean C,
et al. È associata la metilazione epigenetica del promotore del gene alla nascita
successiva adiposità del bambino. Diabete. 2011; 60: 1528 34.
19. McMillen IC, Adam CL, Muhlhausler BS. Origini precoce dell'obesità:
programmazione del sistema di regolazione dell'appetito. J Physiol. 2005; 565 (Pt 1): 9-17.
20. Begum G, Stevens A, Smith EB, Connor K, Challis JR, Bloomfield F, et al.
I cambiamenti epigenetici nei percorsi di regolazione dell'energia ipotalamica fetale sono
associati all'internatoria materna e al gemellaggio. FASEB J.
2012; 26: 1694 703.
21. Ge ZJ, Liang QX, Hou Y, Han ZM, Schatten H, Sun QY, et al. Obesità materna
e il diabete può causare alterazioni della metilazione del DNA negli spermatozoi di
prole in topi. Reprod Biol Endocrinol. 2014; 12: 29.
22. Jousse C, Parry L, Lambert-Langlais S, Maurin AC, Averous J, Bruhat A, et al.
La subnomatizzazione perinatale influenza la metilazione e l'espressione della leptina
gene negli adulti: implicazione per la comprensione della sindrome metabolica.
FASEB J. 2011; 25: 3271 8.
23. Lan X, Cretney EC, Kropp J, Khateeb K, Berg MA, Penagaricano F, et al.
La dieta materna durante la gravidanza induce l'espressione genica e il DNA
cambiamenti di metilazione nei tessuti fetali delle pecore. Genet anteriore. 2013; 4: 49.
24. Li CC, Young PE, Maloney CA, Eaton SA, Cowley MJ, Buckland ME, et al.
L'obesità materna e il diabete inducono difetti metabolici latenti e
cambiamenti epigenetici diffusi nei topi isogenici. Epigenetica. 2013; 8: 602-11.
25. Lillycrop KA, Phillips ES, Jackson AA, Hanson MA, Burdge GC. Proteina dietetica
la restrizione dei ratti in stato di gravidanza induce e l'integrazione dell'acido folico impedisce
modificazione epigenetica dell'espressione genica epatica nella prole. J Nutr.
2005; 135: 1382 6.
26. Radford EJ, Ito M, Shi H, Corish JA, Yamazawa K, Isganaite E, et al. In utero
effetti. In malnutrizione utero perturbs il metilome di sperma adulto
e il metabolismo intergenerazionale. Scienza. 2014; 345 (80): 1255903.
27. Suter M, Bocock P, Showalter L, Hu M, Shope C, McKnight R, et al.
Epigenomica: l'esposizione materna ad alto contenuto di grassi nell'utero interferisce
espressione circadiana periferica nei primati non umani. FASEB J.
2011; 25: 714 26.
28. Suter MA, Ma J, PM Vuguin, Hartil K, Fiallo A, Harris RA, et al. In utero
l'esposizione a una dieta materna ad alto contenuto di grassi altera il codice istone epigenetico in a
modello murino. Am J Obs Gynecol. 2014; 210: 463 e1 463 e11.
29. Tosh DN, Fu Q, Callaway CW, McKnight RA, McMillen IC, Ross MG, et al.
Epigenetica dell'obesità programmata: alterazione del IGF1 epatico in IUGR
l'espressione di mRNA e la struttura degli istoni in rapida e postnatale ritardata
crescita di recupero. Am J Physiol Gastrointest Liver Physiol.
2010; 299: G1023 9.
30. Sandovici I, Smith NH, Nitert MD, Ackers-Johnson M, Uribe-Lewis S, Ito Y,
et al. La dieta materna e l'invecchiamento alterano il controllo epigenetico di un promoter
interazione al gene Hnf4a negli isole pancreatiche del ratto. Proc Natl
Acad Sci US A. 2011; 108: 5449.
31. Braunschweig M, Jagannathan V, Gutzwiller A, Bee G. Ricerche su
risposta transgenerazionale epigenetica lungo la linea maschile nei suini F2. PLoS
Uno. 2012, 7, e30583.
32. Carone BR, Fauquier L, Habib N, Shea JM, Hart CE, Li R, et al. paternamente
indotta dalla riprogettazione ambientale transgenerazionale delle sostanze metaboliche
espressione genica nei mammiferi. Cellula. 2010; 143: 1084 96.
33. Ost A, Lempradl A, Casas E, Weigert M, Tiko T, Deniz M, et al. Dieta paterna
definisce lo stato di cromatina offspring e l'obesità intergenerazionale. Cellula.
2014; 159: 1352 64.
34. Martínez D, Pentinat T, Rib S, Daviaud C, Bloks VW, Cebri J, et al. In utero
la sottovalutazione nei topi maschi programma il metabolismo lipidico del fegato nella seconda generazione
prole che coinvolgono la metilazione alterata di Lxra DNA. Cell Metab.
2014; 19: 941 51.
35. Wei Y, Yang CR, Yi Wei, Zhao ZA, Hou Y, Schatten H, et al. paternamente
indotta dall'eredità transgenerazionale della suscettibilità al diabete
mammiferi. Proc Natl Acad Sci US A. 2014; 111: 1873 8.
36. Grossniklaus U, Kelly WG, Kelly B, Ferguson-Smith AC, Pembrey M, Lindquist
S. Eredità epigenetica transgenerazionale: quanto è importante? Nat Rev
Genet. 2013; 14: 228 35.
37. Pembrey M, Saffery R, Bygren LO. Risposte transgenerative umane a
esperienza precoce: potenziale impatto sullo sviluppo, sulla salute e sulla salute
ricerca biomedica. J Med Genet. 2014; 51: 563 72.
38. Wolff GL, Kodell RL, Moore SR, Cooney CA. Epigenetica materna e metilico
i supplementi influenzano l'espressione del gene agouti nei topi di Avy / a. FASEB J.
1998; 12: 949 57.
39. Jirtle RL, Skinner MK. Epigenomica ambientale e suscettibilità alle malattie.
Nat Rev Genet. 2007; 8: 253.
40. Morgan HD, Sutherland HG, Martin DI, Whitelaw E. Eredità epigenetica a
il locus agouti nel topo. Nat Genet. 1999; 23: 314 8.
41. Cropley JE, Suter CM, Beckman KB, Martin DI. Epigenetico a germi lineari
modifica del murino A vy allele per integrazione nutrizionale. proc
Natl Acad Sci US A. 2006; 103: 17308-12.
42. Hoile SP, Lillycrop KA, Thomas NA, Hanson MA, Burdge GC. Proteina dietetica
la restrizione durante la gravidanza di F0 nei ratti induce i cambiamenti transgenerazionali in
il transcriptome epatico nelle prole femminili. PLoS One. 2011, 6, e21668.
43. Multhaup ML, Seldin MM, Jaffe AE, Lei X, Kirchner H, Mondal P, et al. Mousehuman
l'analisi epigenetica sperimentale disattiva gli obiettivi dietetici e
responsabilità genetica per fenotipi diabetici. Cell Metab. 2015; 21: 138.
44. Michels KB, Binder AM, Dedeurwaerder S, Epstein CB, Greally JM, Gut I, et al.
Raccomandazioni per la progettazione e l'analisi di epigenomi
studi di associazione. Metodi Nat. 2013; 10: 949 55.
45. Dayeh TA, Olsson AH, Volkov P, Almgren P, Rnn T, Ling C. Identificazione di
CpG-SNP associati al diabete di tipo 2 e alla metilazione differenziale del DNA
nelle isole pancreatiche umane. Diabetologia. 2013; 56: 1036 46.
46. Relton CL, Davey Smith G. Randomizzazione epigenetica a due fasi Mendeliana: a
strategia per stabilire il ruolo causale dei processi epigenetici nei percorsi
alla malattia. Int J Epidemiol. 2012; 41: 161 76.
47. Liu Y, Aryee MJ, Padyukov L, Fallin MD, Hesselberg E, Runarsson A, et al.
I dati relativi all'associazione di epigenomi implicano la metilazione del DNA come un
intermediario di rischio genetico nell'artrite reumatoide. Nat Biotechnol.
2013; 31: 142 7.
48. Yuan W, Xia Y, Bell CG, Eppure io, Ferreira T, Ward KJ, et al. Un integrato
analisi epigenomica per locche di suscettibilità del diabete di tipo 2 in monozygotic
Gemelli. Nat Commun. 2014; 5: 5719.
49. Nitert MD, Dayeh T, Volkov P, Elgzyri T, Hall E, Nilsson E, et al. Impatto di un
esercitare l'intervento sulla metilazione del DNA nei muscoli scheletrici da primo grado
parenti di pazienti con diabete di tipo 2. Diabete. 2012; 61: 3322 32.
50. Gagnon F, A ssi D, Carri A, Morange PE, Tr gou t DA. Robusta convalida di
l'associazione di livelli di metilazione al luogo CPT1A con livelli plasmatici lipidi.
J Lipid Res. 2014; 55: 1189 91.
51. Demerath EW, Guan W, Grove ML, Aslibekyan S, Mendelson M, Zhou YH,
et al. Associazione di associazione a livello epigenome (EWAS) del BMI, cambiamento BMI e
la circonferenza della vita negli adulti afro-americani identifica molteplici repliche
loci. Hum Mol Genet. 2015: ddv161 .
52. Dick KJ, Nelson CP, Tsaprouni L, Sandling JK, Assi D, Wahl S, et al. DNA
metilazione e indice di massa corporea: un'analisi su base genomica. Lancetta.
2014; 6736: 1 9.
53. Su S, Zhu H, Xu X, Wang X, Dong Y, Kapuku G, et al. Metilazione del DNA di
il gene LY86 è associato a obesità, resistenza all'insulina e
infiammazione. Twin Res Hum Genet. 2014; 17: 183-91.
54. Clarke-Harris R, Wilkin TJ, Hosking J, Pinkney J, Jeffery AN, Metcalf BS, et al.
PGC1? la metilazione del promotore nel sangue a 5 7 anni predice l'adiposità da
Da 9 a 14 anni (EarlyBird 50). Diabete. 2014; 63: 2528 37.
55. Guay SP, Brisson D, Lamarche B, Biron S, Lescelleur O, Biertho L, et al.
ADRB3 promotore del gene Metilazione del DNA nel sangue e nell'adipo viscerale
il tessuto è associato a disturbi metabolici negli uomini. Epigenomics.
2014; 6: 33 43.
56. Agha G, Houseman EA, Kelsey KT, Eaton CB, Buka SL, Loucks EB. L'adiposità è
associato al profilo di metilazione del DNA nel tessuto adiposo. Int J Epidemiol.
2014: 1.
57. Irvin MR, Zhi D, Joehanes R, Mendelson M, Aslibekyan S, Claas SA, et al.
Studi sull'associazione di epigenomi su digestivi lipidi nel sangue nella genetica di
farmaci ipolipemizzanti e studio di reti dietetiche. Circolazione. 2014; 130: 565 72.
58. Frazier-Wood AC, Aslibekyan S, Absher DM, Hopkins PN, Sha J, Tsai MY, et al.
La metilazione in loco CPT1A è associata alla subfrazione lipoproteina
profili. J Lipid Res. 2014; 55: 1324-30.
59. Pfeifferm L, Wahl S, Pilling LC, Reischl E, Sandling JK, Kunze S, et al. DNA
la metilazione dei geni correlati ai lipidi influenza i livelli lipidici nel sangue. Circ Cardiovasc
Genet. 2015.
60. Petersen AK, Zeilinger S, Kastenm ller G, R misch-Margl W, Brugger M, Peters
A, et al. L'epigenetica si incontra con il metabolomics: un'associazione di epigenomi
studio con i tratti metabolici del siero del sangue. Hum Mol Genet. 2014; 23: 534 45.
61. Hidalgo B, Irvin MR, Sha J, Zhi D, Aslibekyan S, Absher D, et al. Epigenomewide
studio di associazione delle misure di digiuno di glucosio, insulina e HOMA-IR
nella genetica dei farmaci che riducono i lipidi e lo studio della rete dietetica. Diabete.
2014; 63: 801 7.
62. Dayeh T, Volkov P, Salé S, Hall E, Nilsson E, Olsson AH, et al. A livello di genoma
Analisi della metilazione del DNA di isole pancreatiche umane del diabete tipo 2
ei donatori non diabetici identificano i geni candidati che influenzano l'insulina
secrezione. PLoS Genet. 2014, 10, e1004160.
63. Nilsson E, Jansson PA, Perfilyev A, Volkov P, Pedersen M, Svensson MK, et al.
Metilazione alterata del DNA e espressione differenziale di geni che influenzano
metabolismo e infiammazione nel tessuto adiposo da soggetti con tipo 2
diabete. Diabete. 2014; 63: 2962 76.
64. Benton MC, Johnstone A, Eccles D, Harmon B, Hayes MT, Lea RA, et al. L'analisi della metilazione del DNA nel tessuto adiposo umano rivela una modifica differenziale dei geni dell'obesità prima e dopo il bypass gastrico e il peso
perdita. Gene. 2015; 16: 1 21.
65. Bateson P, Gluckman P. La plasticità e la robustezza nello sviluppo e nel
Evoluzione. Int J Epidemiol. 2012; 41: 219.
66. Feinberg AP, Irizarry RA, Feinberg AP, Irizarry RA. Evoluzione nella salute e nella salute
medicina Sackler colloquium: variazione epigenetica stocastica come guida
forza di sviluppo, adattamento evolutivo e malattia. Proc Natl Acad
Sci US A. 2010; 107 (Suppl): 1757-64.
67. Martino D, Loke YJ, Gordon L, Ollikainen M, Cruickshank MN, Saffery R, et al.
Analisi longitudinale su scala genomica della metilazione del DNA nei gemelli dalla nascita
a 18 mesi di età rivela un rapido cambiamento epigenetico nella vita precoce e pairspecific
effetti della discordanza. Genome Biol. 2013; 14: R42.
68. Tobi EW, Goeman JJ, Monajemi R, Gu H, Putter H, Zhang Y, et al. DNA
le firme di metilazione collegano l'esposizione alla carestia prenatale alla crescita e alla
metabolismo. Nat Commun. 2014; 5: 5592.
69. Dominguez-Salas P, Moore SE, Baker MS, Bergen AW, Cox SE, Dyer RA, et al.
L'alimentazione materna alla concezione modula la metilazione del DNA umana
epiallelici metastabili. Nat Commun. 2014; 5: 3746.
70. Quilter CR, Cooper WN, Cliffe KM, Skinner BM, Prentice PM, Nelson L, et al.
Impatto sui modelli di metilazione prole di diabete gestazionale materno
il mellito e la ritenzione della crescita intrauterina suggeriscono i geni comuni e
percorsi legati al successivo rischio di diabete di tipo 2. FASEB J. 2014: 1 12.
71. Morales E, Groom A, Lawlor DA, Relton CL. Marcature di metilazione del DNA in
il sangue del cordone associato all'aumento del peso gestazionale materno: risultati da
la coorte ALSPAC. BMC Res Notes. 2014; 7: 278.
72. Ruchat SM, Houde AA, Voisin G, St-Pierre J, Perron P, Baillargeon JP, et al.
Il diabete mellito gestazionale influenza epigeneticamente prevalentemente i geni
coinvolto nelle malattie metaboliche. Epigenetica. 2013; 8: 935 43.
73. Liu X, Chen Q, Tsai HJ, Wang G, Hong X, Zhou Y, et al. Materno
l'indice di massa corporea di preconzione e il DNA del sangue del midollo spoglio
metilazione: esplorazione delle origini della vita precoce della malattia. Environ Mol
Mutageno. 2014; 55: 223-30.
74. Soubry A, Murphy SK, Wang F., Huang Z, Vidal AC, Fuemmeler BF, et al.
I neonati di genitori obesi hanno alterato i modelli di metilazione del DNA a
geni impressi. Int J Obes (Lond). 2015; 39: 650 7.
75. Jacobsen SC, Brens C, Bork-Jensen J, Ribel-Madsen R, Yang B, Lara E, et al.
Effetti di sovraesposizione ad alto contenuto di grassi a breve termine su DNA a livello genomico
metilazione nel muscolo scheletrico di giovani sani. Diabetologia.
2012; 55: 3341 9.
76. Gillberg L, Jacobsen SC, Rnn T, Brns C, Vaag A. PPARGC1A DNA
metilazione nel tessuto adiposo sottocutaneo in soggetti con basso peso alla nascita
impatto di 5 giorni di sovralimentazione ad alto contenuto di grassi. Metabolismo. 2014; 63: 263 71.
77. Huang YT, Maccani JZJ, Hawley NL, Wing RR, Kelsey KT, McCaffery JM.
Disegni epigenetici in riusciti gestori di perdita di peso: uno studio pilota. Int J
Obes (Lond). 2015; 39: 865 8.
78. Barres R, Kirchner H, Rasmussen M, Yan J, Kantor FR, Krook A, N slund E,
Zierath JR. La perdita di peso dopo l'intervento chirurgico di bypass gastrico nell'obesità umana
rimodella la metilazione del promotore. Cell Rep.2013: 1 8.
79. Ahrens M, Ammerpohl O, von Schnfels W, Kolarova J, Bens S, Itzel T, et al.
L'analisi della metilazione del DNA nella malattia epatica non alcolica del fegato suggerisce
distinte specifiche di malattia e rimodellamento dopo la chirurgia bariatrica.
Cell Metab. 2013; 18: 296-302.
80. Voisin S, Eynon N, Yan X, vescovo DJ. Formazione di esercitazione e metilazione del DNA
negli umani. Acta Physiol (Oxf). 2014; 213: 39.
81. Lindholm ME, Marabita F, Gomez-Cabrero D, Rundqvist H, Ekstr m TJ,
Tegn r J, et al. Un'analisi integrativa rivela una riprogrammazione coordinata
dell'epigenoma e del trascrittome nel muscolo scheletrico umano dopo
formazione. Epigenetica. 2014; 9: 1557 69.
82. Denham J, O'Brien BJ, Marques FZ, Charchar FJ. Cambiamenti nei leucociti
metilome e il suo effetto sui geni correlati cardiovascolari dopo l'esercizio fisico.
J Appl Physiol. 2014: jap.00878.2014.
83. Rowlands DS, pagina RA, Sukala WR, Giri M, Ghimbovschi SD, Hayat I, et al.
Le reti integrate multi-omiche collegano la metilazione del DNA e miRNA
la plasticità muscolare dello scheletro all'esercizio cronico nell'obesità diabetica di tipo 2.
Physiol Genomics. 2014; 46: 747.
84. Horvath S, Erhart W, Brosch M, Ammerpohl O, von Schonfels W, Ahrens M,
et al. L'obesità accelera l'invecchiamento epigenetico del fegato umano. Proc Natl Acad
Sci. 2014; 111: 15538 43.
85. Almn MS, Nilsson EK, Jacobsson JA, Kalnina I, Klovins J, Fredriksson R, et al.
L'analisi genomica rivela i marcatori di metilazione del DNA che variano con
sia l'età che l'obesità. Gene. 2014.; 548: 61 7
86. Houseman EA, Molitor J, Marsit CJ. Regolazioni della miscela delle cellule senza riferimento
nell'analisi dei dati di metilazione del DNA. Bioinformatica. 2014; 30: 1431-9.
87. Wells JC. Una valutazione critica dell'ipotesi di risposta adattativa predittiva.
Int J Epidemiol. 2012; 41: 229 35.
88. Williams-Wyss O, Zhang S, MacLaughlin SM, Kleemann D, Walker SK, Suter
CM, et al. Numero di embrioni e sottovalutazione percepitiva nella
le pecore hanno effetti differenziali sull'epigenotipo surrenale, sulla crescita, e sulla
sviluppo. Sono J Physiol Endocrinol Metab. 2014; 307: E141 50.
89. Zhang S, Rattanatray L, Morrison JL, Nicholas LM, Lie S, McMillen IC.
L'obesità materna e le prime origini dell'obesità infantile: pesa
i benefici e i costi della perdita di peso materno nel periconceptional
periodo per la discendenza. Exp Diabetes Res. 2011; 2011: 585749.
90. Zhang S, Williams-Wyss O, MacLaughlin SM, Walker SK, Kleemann DO, Suter
CM, et al. La sottovalutazione materna durante la prima settimana dopo la concezione
si traduce in una diminuzione dell'espressione del mRNA del recettore del glucocorticoide nel
assenza di ipermetilazione di GR exon 17 nell'ipofisi fetale in ritardo
gestazione. J Dev Orig Heal Dis. 2013; 4: 391 401.
91. Lie S, Morrison JL, Williams-Wyss O, Suter CM, Humphreys DT, Ozanne SE,
et al. I programmi di sopravvivenza percepitivi modificano i segnali di insulina
molecole e microRNA nei muscoli scheletrici in singleton e in due feti
pecore. Biol Reprod. 2014; 90: 5.
92. Van Straten EM, van Meer H, Huijkman NC, van Dijk TH, Baller JF, Verkade
HJ, et al. L'attivazione del recettore del feto al fegato X induce acutamente la lipogenesi ma
non influenza la risposta lipidica al plasma ad una dieta ad alta percentuale di grassi nei topi adulti. Am J
Physiol Endocrinol Metab. 2009; 297: E1171 8.
93. Fernandez-Twinn DS, Alfaradhi MZ, MS Martin-Gronert, Duque-Guimaraes
DE, Piekarz A, Ferland-McCollough D, et al. Downregulation di IRS-1 in
il tessuto adiposo della prole di topi obesi è programmato in modo cellautonomico
attraverso meccanismi post-trascrizionali. Mol Metab.
2014; 3: 325 33.
94. Waterland RA, Travisano M, Tahiliani KG. Ipermetilazione indotta dalla dieta a
l'agouti giallo vitale non è ereditato transgenerazionalmente attraverso la femmina.
FASEB J. 2007; 21: 3380 5.
95. Ge ZJ, Luo SM, Lin F, Liang QX, Huang L, Wei YC, et al. Metilazione del DNA in
oociti e fegato di topi femminili e loro prole: effetti di alto contenuto di grassi-dieta indotta
obesità. Env Heal Perspect. 2014; 122: 159.
96. Ollikainen M, Ismail K, Gervin K, Kyllénen A, Hakkarainen A, Lundbom J, et al.
Alterazioni di metilazione del DNA nel sangue a livello genomico agli elementi regolatori
e regioni eterocromatiche in gemelli monozigoti discordanti per l'obesità
e grasso di fegato. Clin Epigenetics. 2015; 7: 1 13.


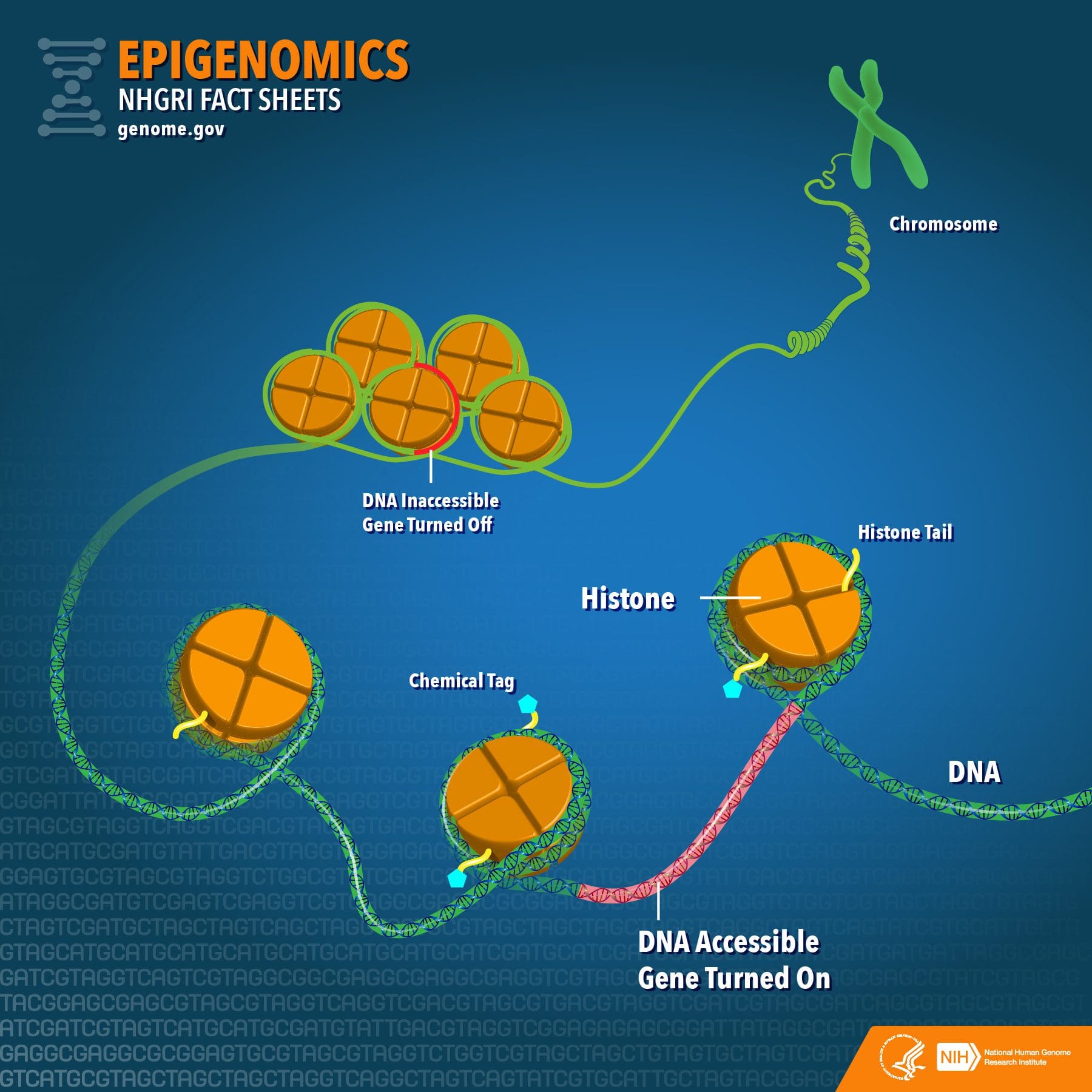
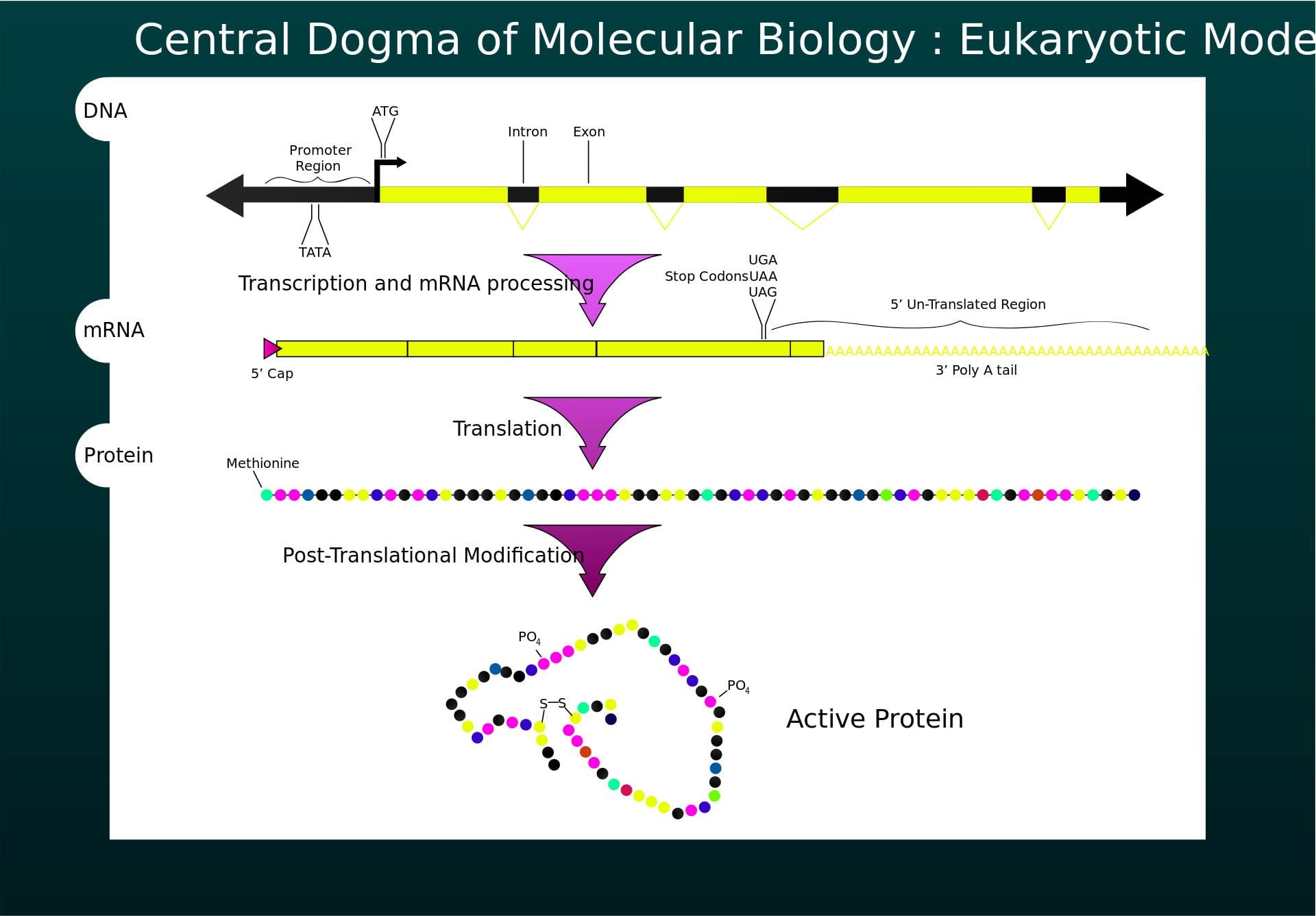




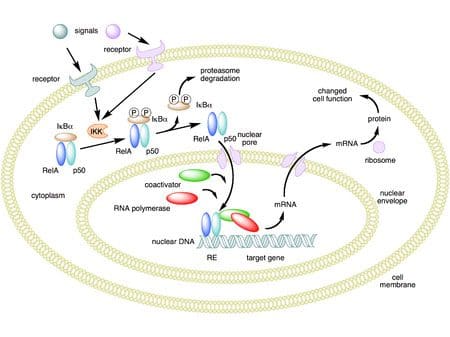

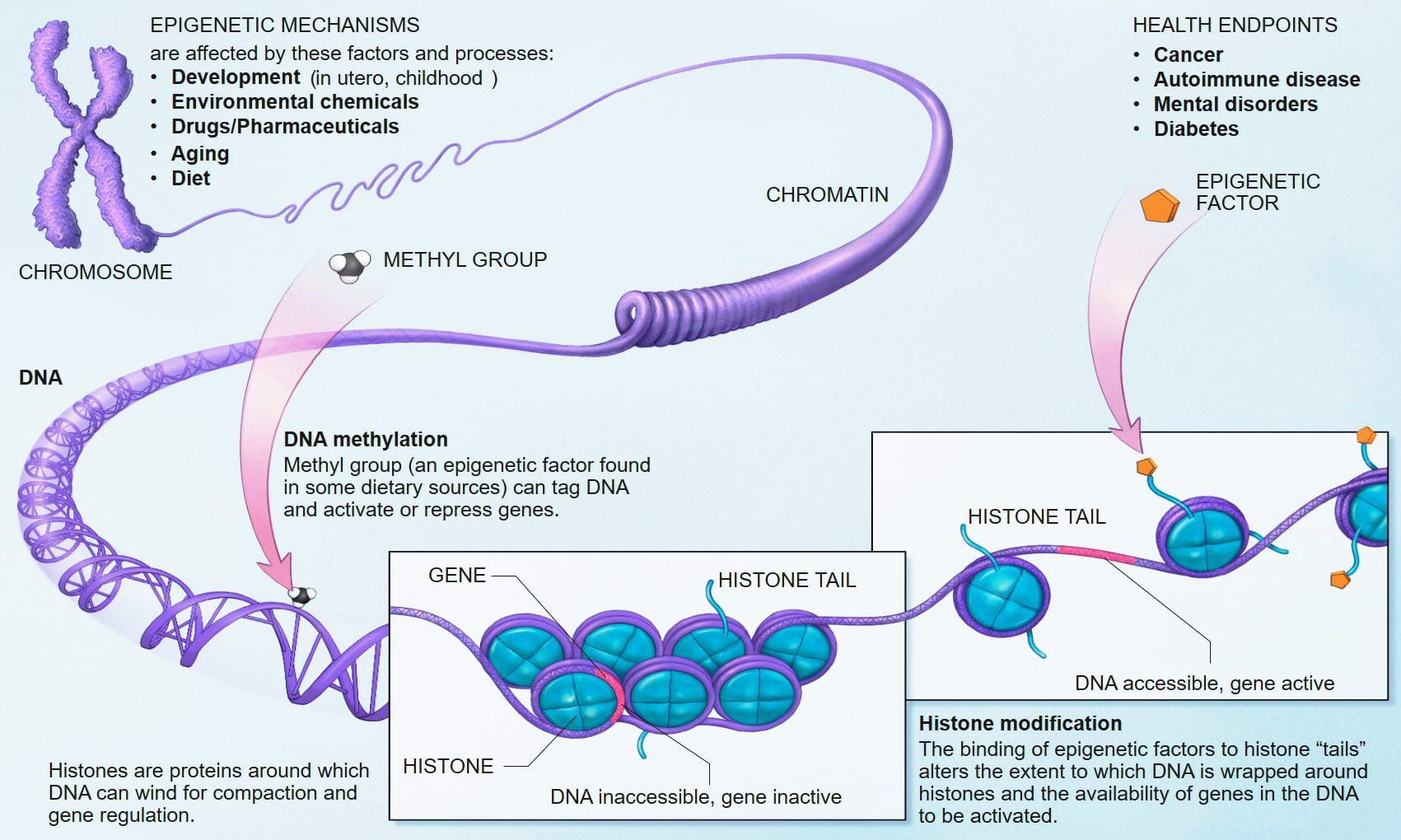




 L'obesità è una malattia complessa e multifattoriale e una migliore comprensione dei meccanismi che sottendono le interazioni tra stile di vita, ambiente e genetica è fondamentale per lo sviluppo di strategie efficaci per la prevenzione e il trattamento [1].
L'obesità è una malattia complessa e multifattoriale e una migliore comprensione dei meccanismi che sottendono le interazioni tra stile di vita, ambiente e genetica è fondamentale per lo sviluppo di strategie efficaci per la prevenzione e il trattamento [1]. I modelli animali offrono opportunità uniche per studi altamente controllati che forniscono informazioni meccanicistiche sul ruolo di specifici segni epigenetici, sia come indicatori dell'attuale stato metabolico che come predittori del futuro rischio di obesità e malattie metaboliche. Un aspetto particolarmente importante degli studi sugli animali è che consentono la valutazione dei cambiamenti epigenetici all'interno dei tessuti bersaglio, inclusi il fegato e l'ipotalamo, che è molto più difficile negli esseri umani. Inoltre, la capacità di raccogliere grandi quantità di tessuto fresco consente di valutare più segni di cromatina così come la metilazione del DNA. Alcune di queste modificazioni epigenetiche, da sole o in combinazione, possono rispondere alla programmazione ambientale. Nei modelli animali, è anche possibile studiare più generazioni di prole e quindi consentire la differenziazione tra trasmissione transgenerazionale e intergenerazionale del rischio di obesità mediata dalla memoria epigenetica dello stato nutrizionale dei genitori, che non può essere facilmente distinta negli studi sull'uomo. Usiamo il primo termine per la trasmissione meiotica del rischio in assenza di esposizione continua, mentre il secondo implica principalmente la trasmissione diretta del rischio attraverso la riprogrammazione metabolica del feto o dei gameti.
I modelli animali offrono opportunità uniche per studi altamente controllati che forniscono informazioni meccanicistiche sul ruolo di specifici segni epigenetici, sia come indicatori dell'attuale stato metabolico che come predittori del futuro rischio di obesità e malattie metaboliche. Un aspetto particolarmente importante degli studi sugli animali è che consentono la valutazione dei cambiamenti epigenetici all'interno dei tessuti bersaglio, inclusi il fegato e l'ipotalamo, che è molto più difficile negli esseri umani. Inoltre, la capacità di raccogliere grandi quantità di tessuto fresco consente di valutare più segni di cromatina così come la metilazione del DNA. Alcune di queste modificazioni epigenetiche, da sole o in combinazione, possono rispondere alla programmazione ambientale. Nei modelli animali, è anche possibile studiare più generazioni di prole e quindi consentire la differenziazione tra trasmissione transgenerazionale e intergenerazionale del rischio di obesità mediata dalla memoria epigenetica dello stato nutrizionale dei genitori, che non può essere facilmente distinta negli studi sull'uomo. Usiamo il primo termine per la trasmissione meiotica del rischio in assenza di esposizione continua, mentre il secondo implica principalmente la trasmissione diretta del rischio attraverso la riprogrammazione metabolica del feto o dei gameti.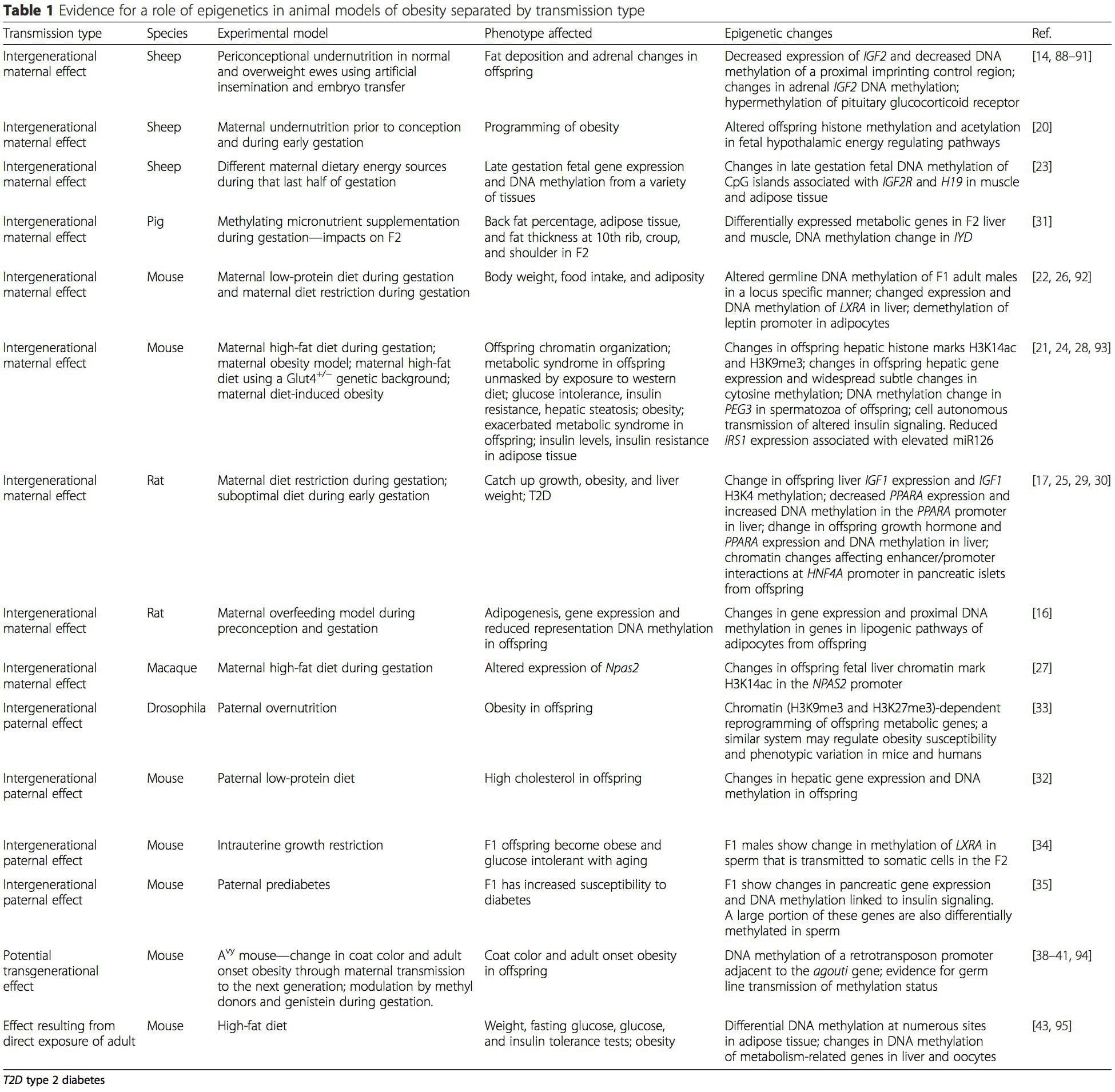 i) Cambiamenti epigenetici nella prole associata all'alimentazione materna durante la gestazione
i) Cambiamenti epigenetici nella prole associata all'alimentazione materna durante la gestazione L'integrazione nutrizionale materna, la denutrizione e la sovralimentazione durante la gravidanza possono alterare la deposizione di grasso e l'omeostasi energetica nella prole [11, 13-15, 19]. Associati a questi effetti nella prole sono i cambiamenti nella metilazione del DNA, le modificazioni post-traduzionali degli istoni e l'espressione genica per diversi geni bersaglio, specialmente i geni che regolano il metabolismo degli acidi grassi e la segnalazione dell'insulina [16, 17, 20-30]. La diversità dei modelli animali utilizzati in questi studi e le vie metaboliche comuni influenzate suggeriscono una risposta adattativa conservata dal punto di vista evolutivo mediata dalla modificazione epigenetica. Tuttavia, alcuni dei geni specifici identificati e dei cambiamenti epigenetici sono stati convalidati in modo incrociato in studi correlati e le indagini su larga scala a livello di genoma in genere non sono state applicate. Uno dei principali ostacoli al confronto di questi studi è rappresentato dalle diverse finestre mentali di sviluppo soggette a sfide nutrizionali, che possono causare risultati notevolmente diversi. È anche richiesta la prova che i cambiamenti epigenetici sono causali piuttosto che essere associati a cambiamenti fenotipici della prole. Ciò richiederà l'identificazione di una risposta epigenetica `` memoria '' nutrizionalmente indotta dai genitori che precede lo sviluppo del fenotipo alterato nella prole.
L'integrazione nutrizionale materna, la denutrizione e la sovralimentazione durante la gravidanza possono alterare la deposizione di grasso e l'omeostasi energetica nella prole [11, 13-15, 19]. Associati a questi effetti nella prole sono i cambiamenti nella metilazione del DNA, le modificazioni post-traduzionali degli istoni e l'espressione genica per diversi geni bersaglio, specialmente i geni che regolano il metabolismo degli acidi grassi e la segnalazione dell'insulina [16, 17, 20-30]. La diversità dei modelli animali utilizzati in questi studi e le vie metaboliche comuni influenzate suggeriscono una risposta adattativa conservata dal punto di vista evolutivo mediata dalla modificazione epigenetica. Tuttavia, alcuni dei geni specifici identificati e dei cambiamenti epigenetici sono stati convalidati in modo incrociato in studi correlati e le indagini su larga scala a livello di genoma in genere non sono state applicate. Uno dei principali ostacoli al confronto di questi studi è rappresentato dalle diverse finestre mentali di sviluppo soggette a sfide nutrizionali, che possono causare risultati notevolmente diversi. È anche richiesta la prova che i cambiamenti epigenetici sono causali piuttosto che essere associati a cambiamenti fenotipici della prole. Ciò richiederà l'identificazione di una risposta epigenetica `` memoria '' nutrizionalmente indotta dai genitori che precede lo sviluppo del fenotipo alterato nella prole. Studi emergenti hanno dimostrato che il piano nutrizionale paterno può influire sulla deposizione di grasso della prole e sui segni epigenetici [31-34]. Una recente indagine su topi ha dimostrato che il pre-diabete paterno porta ad una maggiore suscettibilità al diabete nella prole F1 con cambiamenti associati nell'espressione genica pancreatica e metilazione del DNA legata alla segnalazione dell'insulina [35]. È importante sottolineare che c'era una sovrapposizione di questi cambiamenti epigenetici nelle isole pancreatiche e negli spermatozoi che suggerivano l'ereditarietà della linea germinale. Tuttavia, la maggior parte di questi studi, sebbene intriganti nelle loro implicazioni, sono limitati nella scala genomica di indagine e mostrano frequentemente alterazioni epigenetiche deboli e alquanto transitorie associate a fenotipi metabolici lievi nella prole.
Studi emergenti hanno dimostrato che il piano nutrizionale paterno può influire sulla deposizione di grasso della prole e sui segni epigenetici [31-34]. Una recente indagine su topi ha dimostrato che il pre-diabete paterno porta ad una maggiore suscettibilità al diabete nella prole F1 con cambiamenti associati nell'espressione genica pancreatica e metilazione del DNA legata alla segnalazione dell'insulina [35]. È importante sottolineare che c'era una sovrapposizione di questi cambiamenti epigenetici nelle isole pancreatiche e negli spermatozoi che suggerivano l'ereditarietà della linea germinale. Tuttavia, la maggior parte di questi studi, sebbene intriganti nelle loro implicazioni, sono limitati nella scala genomica di indagine e mostrano frequentemente alterazioni epigenetiche deboli e alquanto transitorie associate a fenotipi metabolici lievi nella prole.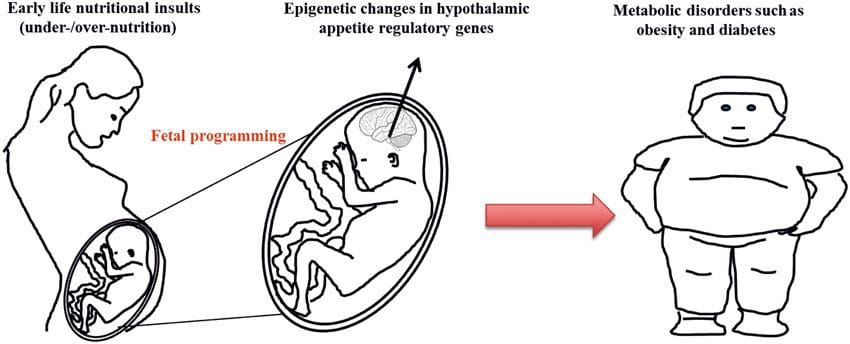 La trasmissione stabile di informazioni epigenetiche tra più generazioni è ben descritta nei sistemi vegetali e in C. elegans, ma il suo significato nei mammiferi è ancora molto dibattuto [36, 37]. Una base epigenetica per la trasmissione non genitoriale dei fenotipi in risposta alle esposizioni alimentari è stata ben stabilita, anche nelle specie di bestiame [31]. Gli studi più influenti che dimostrano gli effetti della trasmissione epigenetica sul fenotipo della prole hanno utilizzato l'esempio del topo agouti giallo (Avy) vitale [38]. In questo topo, l'inserimento di un retrotrasposone a monte del gene agouti provoca la sua espressione costitutiva e il conseguente colore del mantello giallo e l'obesità ad esordio nell'adulto. La trasmissione materna attraverso la linea germinale si traduce in un silenziamento mediato dalla metilazione del DNA dell'espressione di agouti con conseguente colore del mantello wild-type e fenotipo magro della prole [39, 40]. È importante sottolineare che studi successivi su questi topi hanno dimostrato che l'esposizione materna a donatori di metile provoca un cambiamento nel colore del mantello [41]. Uno studio ha riportato la trasmissione di un fenotipo alla generazione F3 e alterazioni nell'espressione di un gran numero di geni in risposta alla restrizione proteica in F0 [42]; tuttavia, le alterazioni nell'espressione erano altamente variabili e un collegamento diretto ai cambiamenti epigenetici non è stato identificato in questo sistema.
La trasmissione stabile di informazioni epigenetiche tra più generazioni è ben descritta nei sistemi vegetali e in C. elegans, ma il suo significato nei mammiferi è ancora molto dibattuto [36, 37]. Una base epigenetica per la trasmissione non genitoriale dei fenotipi in risposta alle esposizioni alimentari è stata ben stabilita, anche nelle specie di bestiame [31]. Gli studi più influenti che dimostrano gli effetti della trasmissione epigenetica sul fenotipo della prole hanno utilizzato l'esempio del topo agouti giallo (Avy) vitale [38]. In questo topo, l'inserimento di un retrotrasposone a monte del gene agouti provoca la sua espressione costitutiva e il conseguente colore del mantello giallo e l'obesità ad esordio nell'adulto. La trasmissione materna attraverso la linea germinale si traduce in un silenziamento mediato dalla metilazione del DNA dell'espressione di agouti con conseguente colore del mantello wild-type e fenotipo magro della prole [39, 40]. È importante sottolineare che studi successivi su questi topi hanno dimostrato che l'esposizione materna a donatori di metile provoca un cambiamento nel colore del mantello [41]. Uno studio ha riportato la trasmissione di un fenotipo alla generazione F3 e alterazioni nell'espressione di un gran numero di geni in risposta alla restrizione proteica in F0 [42]; tuttavia, le alterazioni nell'espressione erano altamente variabili e un collegamento diretto ai cambiamenti epigenetici non è stato identificato in questo sistema.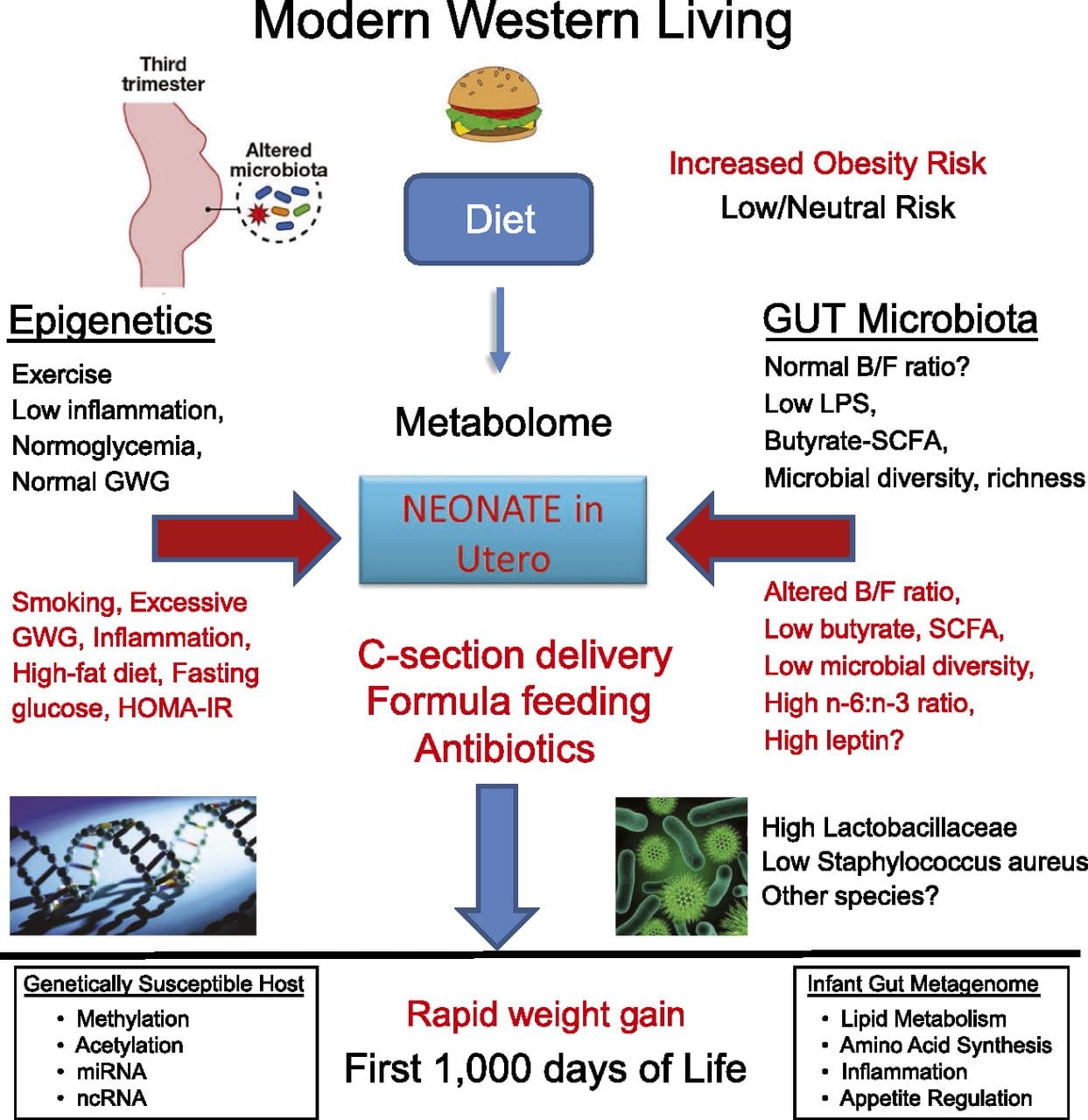 Mentre molti studi hanno individuato cambiamenti epigenetici associati alla dieta nei modelli animali che utilizzano aree candidate specifiche del sito, sono state eseguite alcune analisi genomiche. Un recente studio si è concentrato sulla determinazione dell'impatto epigenetico diretto delle diete ad alto tenore di grassi / obesità indotta dalla dieta nei topi adulti utilizzando l'espressione genica di genoma e le analisi della metilazione del DNA [43]. Questo studio ha individuato le regioni 232 differenzialmente metilate (DMR) in adipociti dal controllo e dai topi alimentati ad alto contenuto di grassi. Importante, le regioni umane corrispondenti per i DMR murine sono state anche differenzialmente metilate nei tessuti adiposi da una popolazione di persone obese e magre, evidenziando così la notevole conservazione evolutiva di queste regioni. Questo risultato sottolinea la probabile importanza dei DMR identificati nella regolazione dell'omeostasi di energia nei mammiferi.
Mentre molti studi hanno individuato cambiamenti epigenetici associati alla dieta nei modelli animali che utilizzano aree candidate specifiche del sito, sono state eseguite alcune analisi genomiche. Un recente studio si è concentrato sulla determinazione dell'impatto epigenetico diretto delle diete ad alto tenore di grassi / obesità indotta dalla dieta nei topi adulti utilizzando l'espressione genica di genoma e le analisi della metilazione del DNA [43]. Questo studio ha individuato le regioni 232 differenzialmente metilate (DMR) in adipociti dal controllo e dai topi alimentati ad alto contenuto di grassi. Importante, le regioni umane corrispondenti per i DMR murine sono state anche differenzialmente metilate nei tessuti adiposi da una popolazione di persone obese e magre, evidenziando così la notevole conservazione evolutiva di queste regioni. Questo risultato sottolinea la probabile importanza dei DMR identificati nella regolazione dell'omeostasi di energia nei mammiferi.
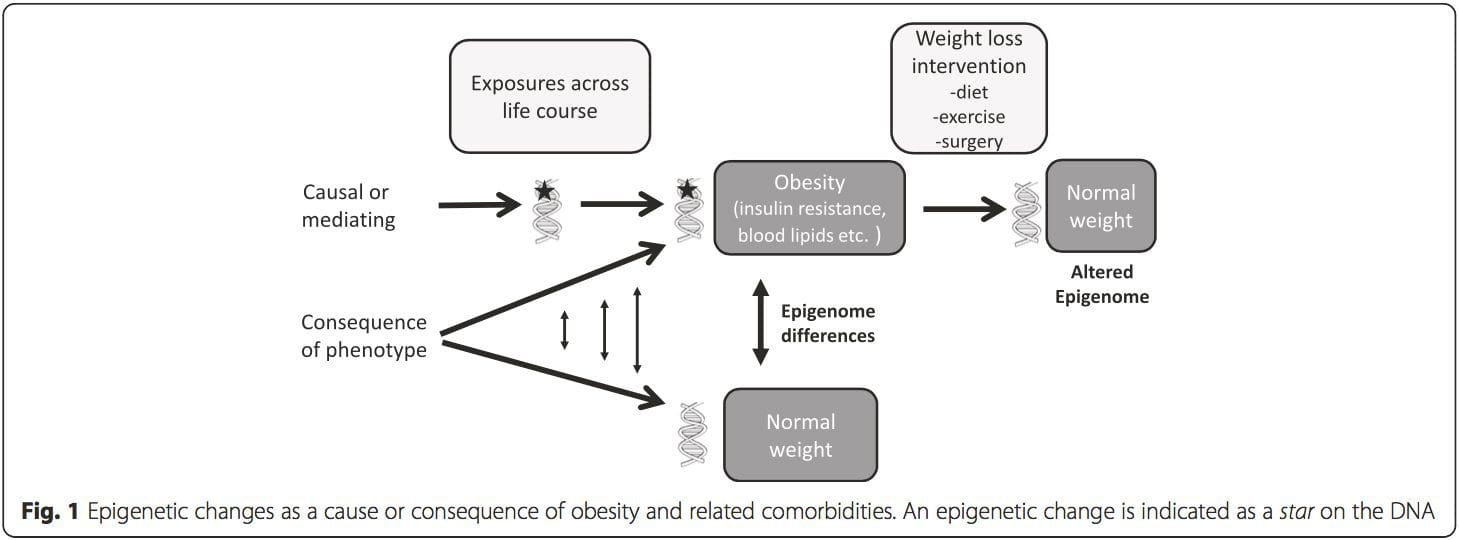 (i) Studi di associazione genetica. I polimorfismi genetici che sono associati ad un aumentato rischio di sviluppare particolari condizioni sono a priori legati ai geni causali. La presenza di metilazione differenziale in tali regioni inferisce la rilevanza funzionale di questi cambiamenti epigenetici nel controllo dell'espressione dei geni prossimali. Esistono forti effetti genetici ad azione cis alla base di molte variazioni epigenetiche [7, 45] e negli studi basati sulla popolazione sono stati applicati metodi che utilizzano surrogati genetici per inferire un ruolo causale o mediatore delle differenze epigenomiche [7, 46-48] . L'uso di informazioni genetiche familiari può anche portare all'identificazione di regioni candidate potenzialmente causali che mostrano una metilazione differenziale correlata al fenotipo [49].
(i) Studi di associazione genetica. I polimorfismi genetici che sono associati ad un aumentato rischio di sviluppare particolari condizioni sono a priori legati ai geni causali. La presenza di metilazione differenziale in tali regioni inferisce la rilevanza funzionale di questi cambiamenti epigenetici nel controllo dell'espressione dei geni prossimali. Esistono forti effetti genetici ad azione cis alla base di molte variazioni epigenetiche [7, 45] e negli studi basati sulla popolazione sono stati applicati metodi che utilizzano surrogati genetici per inferire un ruolo causale o mediatore delle differenze epigenomiche [7, 46-48] . L'uso di informazioni genetiche familiari può anche portare all'identificazione di regioni candidate potenzialmente causali che mostrano una metilazione differenziale correlata al fenotipo [49].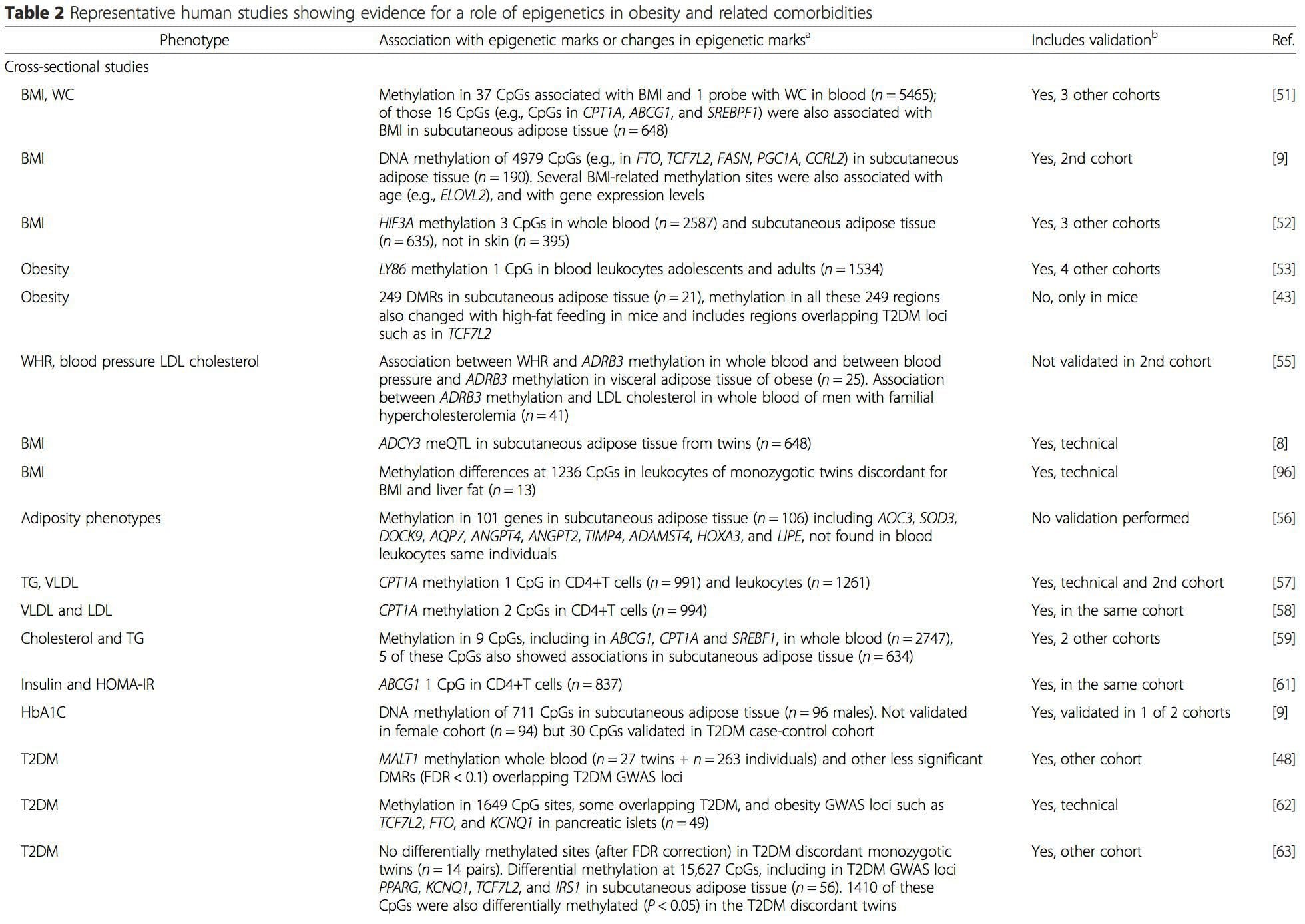
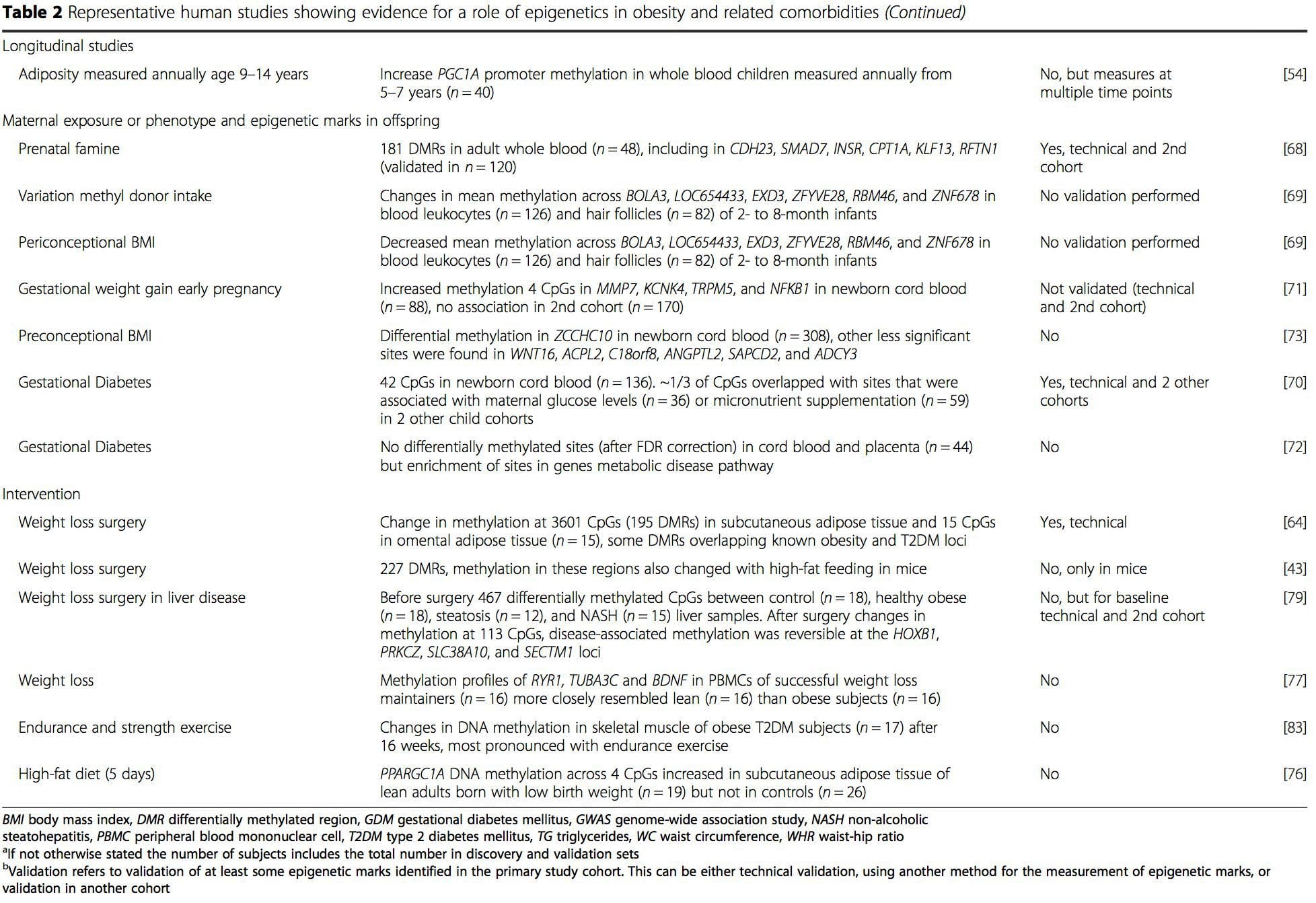 Da questi studi, la metilazione alterata di PGC1A, HIF3A, ABCG1 e CPT1A e la RXRA [18] descritta in precedenza sono emerse come biomarcatori associati, o forse predittivi, alla salute metabolica che sono anche candidati plausibili per un ruolo nello sviluppo della malattia metabolica .
Da questi studi, la metilazione alterata di PGC1A, HIF3A, ABCG1 e CPT1A e la RXRA [18] descritta in precedenza sono emerse come biomarcatori associati, o forse predittivi, alla salute metabolica che sono anche candidati plausibili per un ruolo nello sviluppo della malattia metabolica .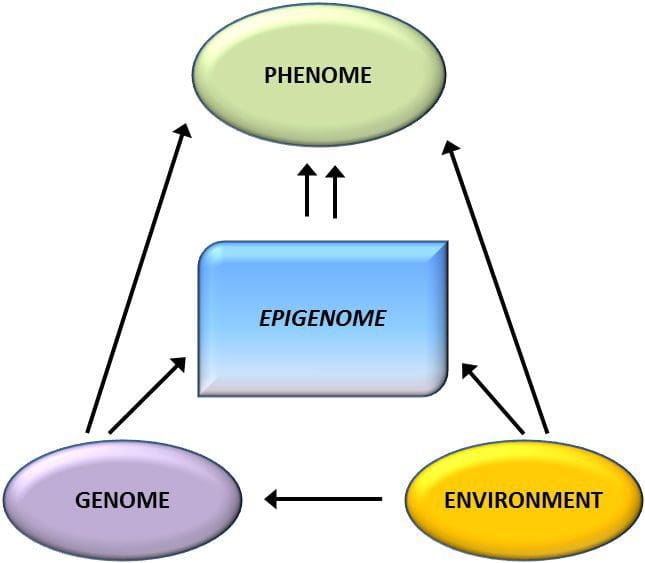 La variazione epigenetica è fortemente influenzata dalla variazione genetica sottostante, con il genotipo stimato per spiegare ~ 20-40% della variazione [6, 8]. Recentemente, una serie di studi ha iniziato a integrare i dati del metiloma e del genotipo per identificare i loci dei tratti quantitativi di metilazione (meQTL) associati ai fenotipi della malattia. Ad esempio, nel tessuto adiposo, è stata identificata una sovrapposizione meQTL con un locus di rischio genetico BMI in un elemento potenziatore a monte di ADCY3 [8]. Altri studi hanno anche identificato sovrapposizioni tra obesità nota e loci di rischio T2DM e DMR associati all'obesità e T2DM [43, 48, 62]. La metilazione di un certo numero di tali DMR è stata modulata anche dall'alimentazione ad alto contenuto di grassi nei topi [43] e dalla perdita di peso negli esseri umani [64]. Questi risultati identificano un legame intrigante tra le variazioni genetiche legate alla suscettibilità alla malattia e la loro associazione con regioni del genoma che subiscono modificazioni epigenetiche in risposta a sfide nutrizionali, implicando una relazione causale. La stretta connessione tra variazione genetica ed epigenetica può significare i loro ruoli essenziali nella generazione della variazione individuale [65, 66]. Tuttavia, mentre questi risultati suggeriscono che la metilazione del DNA può essere un mediatore di effetti genetici, è anche importante considerare che i processi genetici ed epigenetici potrebbero agire indipendentemente sugli stessi geni. Studi sui gemelli [8, 63, 67] possono fornire importanti intuizioni e indicare che le differenze interindividuali nei livelli di metilazione del DNA derivano prevalentemente da ambienti non condivisi e influenze stocastiche, in minima parte da effetti ambientali condivisi, ma anche con un impatto significativo della genetica variazione.
La variazione epigenetica è fortemente influenzata dalla variazione genetica sottostante, con il genotipo stimato per spiegare ~ 20-40% della variazione [6, 8]. Recentemente, una serie di studi ha iniziato a integrare i dati del metiloma e del genotipo per identificare i loci dei tratti quantitativi di metilazione (meQTL) associati ai fenotipi della malattia. Ad esempio, nel tessuto adiposo, è stata identificata una sovrapposizione meQTL con un locus di rischio genetico BMI in un elemento potenziatore a monte di ADCY3 [8]. Altri studi hanno anche identificato sovrapposizioni tra obesità nota e loci di rischio T2DM e DMR associati all'obesità e T2DM [43, 48, 62]. La metilazione di un certo numero di tali DMR è stata modulata anche dall'alimentazione ad alto contenuto di grassi nei topi [43] e dalla perdita di peso negli esseri umani [64]. Questi risultati identificano un legame intrigante tra le variazioni genetiche legate alla suscettibilità alla malattia e la loro associazione con regioni del genoma che subiscono modificazioni epigenetiche in risposta a sfide nutrizionali, implicando una relazione causale. La stretta connessione tra variazione genetica ed epigenetica può significare i loro ruoli essenziali nella generazione della variazione individuale [65, 66]. Tuttavia, mentre questi risultati suggeriscono che la metilazione del DNA può essere un mediatore di effetti genetici, è anche importante considerare che i processi genetici ed epigenetici potrebbero agire indipendentemente sugli stessi geni. Studi sui gemelli [8, 63, 67] possono fornire importanti intuizioni e indicare che le differenze interindividuali nei livelli di metilazione del DNA derivano prevalentemente da ambienti non condivisi e influenze stocastiche, in minima parte da effetti ambientali condivisi, ma anche con un impatto significativo della genetica variazione. Ambiente prenatale: Due studi pubblicati di recente hanno fatto uso di popolazioni umane che hanno sperimentato variazioni "naturali" nell'apporto di nutrienti per studiare l'impatto della nutrizione materna prima o durante la gravidanza sulla metilazione del DNA nella prole [68, 69]. Il primo studio ha utilizzato una coorte madre-figlio del Gambia per dimostrare che sia le variazioni stagionali dell'assunzione di donatori di metile materno durante la gravidanza che il BMI materno pre-gravidanza erano associati a metilazione alterata nei neonati [69]. Il secondo studio ha utilizzato la prole adulta della coorte olandese Hunger Winter per studiare l'effetto dell'esposizione prenatale a un periodo acuto di grave denutrizione materna sulla metilazione del DNA dei geni coinvolti nella crescita e nel metabolismo in età adulta [68]. I risultati hanno evidenziato l'importanza della tempistica dell'esposizione nel suo impatto sull'epigenoma, poiché effetti epigenetici significativi sono stati identificati solo in individui esposti alla carestia durante le prime fasi della gestazione. È importante sottolineare che i cambiamenti epigenetici si sono verificati in concomitanza con un aumento del BMI; tuttavia, non è stato possibile stabilire in questo studio se questi cambiamenti fossero presenti in una fase precoce della vita o come conseguenza di un BMI più elevato.
Ambiente prenatale: Due studi pubblicati di recente hanno fatto uso di popolazioni umane che hanno sperimentato variazioni "naturali" nell'apporto di nutrienti per studiare l'impatto della nutrizione materna prima o durante la gravidanza sulla metilazione del DNA nella prole [68, 69]. Il primo studio ha utilizzato una coorte madre-figlio del Gambia per dimostrare che sia le variazioni stagionali dell'assunzione di donatori di metile materno durante la gravidanza che il BMI materno pre-gravidanza erano associati a metilazione alterata nei neonati [69]. Il secondo studio ha utilizzato la prole adulta della coorte olandese Hunger Winter per studiare l'effetto dell'esposizione prenatale a un periodo acuto di grave denutrizione materna sulla metilazione del DNA dei geni coinvolti nella crescita e nel metabolismo in età adulta [68]. I risultati hanno evidenziato l'importanza della tempistica dell'esposizione nel suo impatto sull'epigenoma, poiché effetti epigenetici significativi sono stati identificati solo in individui esposti alla carestia durante le prime fasi della gestazione. È importante sottolineare che i cambiamenti epigenetici si sono verificati in concomitanza con un aumento del BMI; tuttavia, non è stato possibile stabilire in questo studio se questi cambiamenti fossero presenti in una fase precoce della vita o come conseguenza di un BMI più elevato. Ambiente postnatale: L'epigenoma viene stabilito de novo durante lo sviluppo embrionale e quindi l'ambiente prenatale ha molto probabilmente l'impatto più significativo sull'epigenoma. Tuttavia, è ora chiaro che i cambiamenti si verificano nell'epigenoma `` maturo '' sotto l'influenza di una serie di condizioni, tra cui l'invecchiamento, l'esposizione alle tossine e le alterazioni della dieta. Ad esempio, sono stati dimostrati cambiamenti nella metilazione del DNA in numerosi geni nel muscolo scheletrico e PGC1A nel tessuto adiposo in risposta a una dieta ricca di grassi [75, 76]. Anche gli interventi per perdere massa grassa sono stati associati a cambiamenti nella metilazione del DNA. Studi hanno riportato che i profili di metilazione del DNA del tessuto adiposo [43, 64], delle cellule mononucleate del sangue periferico [77] e del tessuto muscolare [78] nei pazienti precedentemente obesi diventano più simili ai profili dei soggetti magri dopo la perdita di peso. La chirurgia per la perdita di peso ha anche parzialmente invertito i cambiamenti di metilazione associati alla steatosi epatica non alcolica nel fegato [79] e in un altro studio ha portato all'ipometilazione di più geni candidati all'obesità, con effetti più pronunciati nel sottocutaneo rispetto al grasso omentale (viscerale) [64] . L'accumulo di prove suggerisce che gli interventi di esercizio fisico possono anche influenzare la metilazione del DNA. La maggior parte di questi studi sono stati condotti su individui magri [80-82], ma uno studio sull'esercizio su soggetti obesi con T2DM ha anche dimostrato cambiamenti nella metilazione del DNA, inclusi i geni coinvolti nel trasporto degli acidi grassi e del glucosio [83]. I cambiamenti epigenetici si verificano anche con l'invecchiamento e dati recenti suggeriscono un ruolo dell'obesità nell'aumentarli [9, 84, 85]. L'obesità ha accelerato l'età epigenetica del tessuto epatico, ma in contrasto con i risultati sopra descritti, questo effetto non era reversibile dopo la perdita di peso [84].
Ambiente postnatale: L'epigenoma viene stabilito de novo durante lo sviluppo embrionale e quindi l'ambiente prenatale ha molto probabilmente l'impatto più significativo sull'epigenoma. Tuttavia, è ora chiaro che i cambiamenti si verificano nell'epigenoma `` maturo '' sotto l'influenza di una serie di condizioni, tra cui l'invecchiamento, l'esposizione alle tossine e le alterazioni della dieta. Ad esempio, sono stati dimostrati cambiamenti nella metilazione del DNA in numerosi geni nel muscolo scheletrico e PGC1A nel tessuto adiposo in risposta a una dieta ricca di grassi [75, 76]. Anche gli interventi per perdere massa grassa sono stati associati a cambiamenti nella metilazione del DNA. Studi hanno riportato che i profili di metilazione del DNA del tessuto adiposo [43, 64], delle cellule mononucleate del sangue periferico [77] e del tessuto muscolare [78] nei pazienti precedentemente obesi diventano più simili ai profili dei soggetti magri dopo la perdita di peso. La chirurgia per la perdita di peso ha anche parzialmente invertito i cambiamenti di metilazione associati alla steatosi epatica non alcolica nel fegato [79] e in un altro studio ha portato all'ipometilazione di più geni candidati all'obesità, con effetti più pronunciati nel sottocutaneo rispetto al grasso omentale (viscerale) [64] . L'accumulo di prove suggerisce che gli interventi di esercizio fisico possono anche influenzare la metilazione del DNA. La maggior parte di questi studi sono stati condotti su individui magri [80-82], ma uno studio sull'esercizio su soggetti obesi con T2DM ha anche dimostrato cambiamenti nella metilazione del DNA, inclusi i geni coinvolti nel trasporto degli acidi grassi e del glucosio [83]. I cambiamenti epigenetici si verificano anche con l'invecchiamento e dati recenti suggeriscono un ruolo dell'obesità nell'aumentarli [9, 84, 85]. L'obesità ha accelerato l'età epigenetica del tessuto epatico, ma in contrasto con i risultati sopra descritti, questo effetto non era reversibile dopo la perdita di peso [84].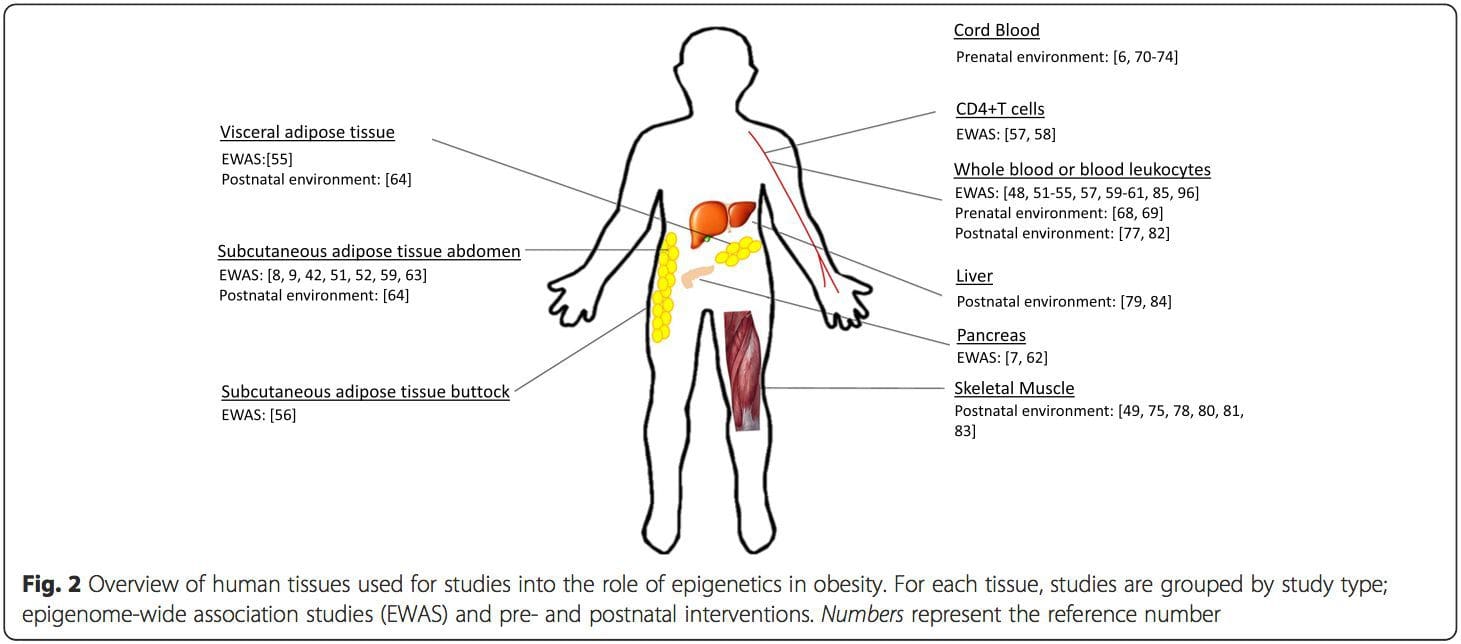 Conclusioni
Conclusioni



